Chapter 5: 단백질 구조·상호작용 예측 — AlphaFold 이후의 효능 모델링
왜 이 챕터인가
Chapter 4가 "후보 분자·균주의 우선순위 매기기"를 다뤘다면, 이 챕터는 한 단계 더 깊이 들어간다. 그 후보 분자가 피부 단백질의 어느 자리에 어떻게 결합하는가를 in silico로 추적하는 단계다. 화장품 효능의 90% 이상은 결국 단백질-분자 상호작용으로 환원된다 — 콜라겐의 합성·분해(MMP-1·MMP-9), 피부 장벽의 분화(필라그린·AHR), 염증(NF-κB·AHR·NRF2), 색소(타이로시나아제·MITF), 각질 박리(KLK5·KLK7 카르밀상피혹스 family). 결합 자리(binding pocket)의 기하·전자 구조를 알면 효능을 예측할 수 있고, 모르면 발효액을 만들어 세포에 뿌리고 결과를 기다리는 1세대 방식으로 회귀한다.
2021년 7월 AlphaFold2가 발표되기 전까지 단백질 구조 예측은 박사학위 한 편이 들어가는 일이었다. CASP14에서 [14]이 보고한 평균 GDT-TS 87.0(중간값 92.4)은 X-ray 결정학의 실험 오차 범위(~1Å)에 진입한 첫 계산 결과였다. 그로부터 4년 만에 단백질 구조 한 개의 예측 비용은 GPU 몇 분으로 떨어졌고, 단백질-리간드 복합체 예측(AlphaFold 3, Boltz-1, Chai-1)이 2024년 한 해에 commodity로 풀렸다. 이 챕터는 그 변곡점의 정확한 토폴로지를 정리하고, 화장품 R&D에 어떤 의미를 갖는지 — 그리고 무엇이 아직 안 풀렸는지 — 따로 분리한다.
이 챕터의 정량적 핵심 3가지 1. CASP14에서 AlphaFold2의 중간값 GDT-TS 92.4 [14] — 결정학 오차 수준에 진입한 첫 계산 모델. 이전 세대 1위는 GDT-TS ~65 수준에 그쳤다. 2. 2024년 4–11월 사이 AlphaFold 3 → RoseTTAFold All-Atom → Boltz-1 → Chai-1이 연속 공개되며 단백질-리간드 복합체 예측이 폐쇄형·오픈형 모두에서 commodity화. [1], [16], [22], [4]. 3. 화장품 산업의 활용은 아직 동료 심사 readout 0건 (Gap 1). 비교 가능한 인접 산업 readout은 [13]의 rentosertib 임상 2a — 표적 발굴부터 IND까지 30개월. 화장품의 첫 발표 readout은 이 템플릿을 빌릴 가능성이 높다 (Chapter 9, Chapter 11과 직결).
5.1 왜 구조 예측이 화장품에서 중요한가
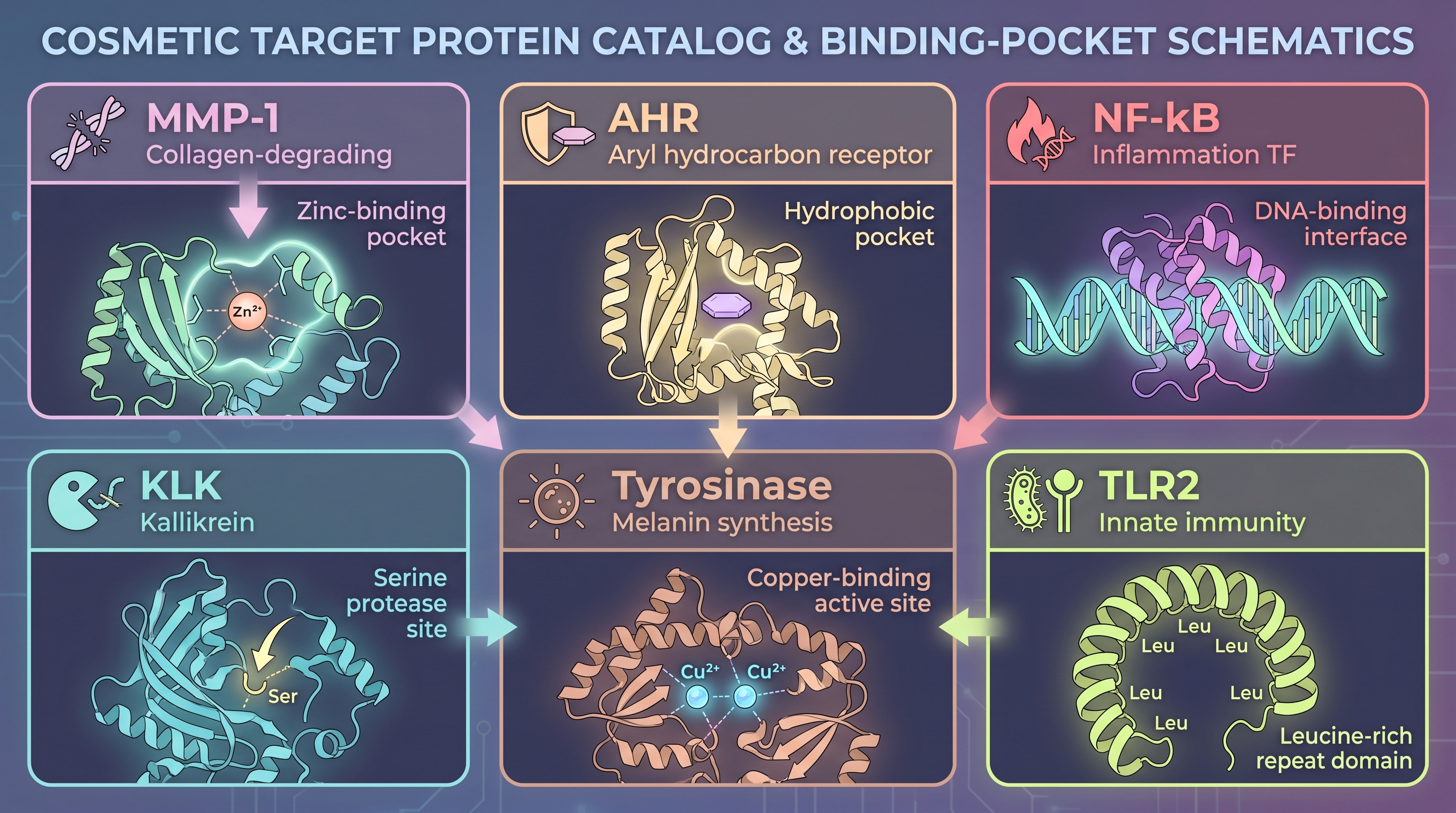
먼저 화장품 활성 성분이 표적으로 삼는 단백질의 목록을 보자. 거의 모든 화장품 R&D 카탈로그는 같은 단백질군으로 수렴한다.
- 콜라겐·엘라스틴 합성 축: COL1A1, COL3A1, ELN, LOX. 합성 자체는 ribosome 산물이지만 분해를 막는 것이 효능 메커니즘의 핵심.
- MMP family(matrix metalloproteinase): MMP-1 (collagenase-1), MMP-3, MMP-9. UV·노화로 활성이 올라가며 콜라겐을 분해한다. 화장품 항노화 활성 성분의 절반 이상이 MMP-1/9 억제를 1차 endpoint로 삼는다.
- AHR(aryl hydrocarbon receptor): 피부 장벽 분화(필라그린·로리크린·인볼루크린 발현)와 항염을 동시에 조절. [21]가 Galactomyces ferment filtrate(SK-II Pitera 원료)의 작동 기전을 푼 자리.
- NF-κB·NRF2 축: 염증과 산화 스트레스 응답의 핵심 transcription factor. [10]가 같은 Galactomyces filtrate의 두 번째 분자 기둥으로 NRF2 활성화를 보였다.
- 카르밀상피혹스 단백질 가수분해효소(kallikrein, KLK5·KLK7): 각질 박리 조절. 아토피·로사시아에서 활성 이상.
- 타이로시나아제·MITF 축: 멜라닌 생합성. 미백 endpoint의 핵심 표적.
- 피부 GPCR과 인테그린: TLR2, TRPV1, PAR2 등. 미생물 신호 인식과 통증·가려움 sensing.
핵심 관찰: 이 단백질 대부분은 세포 표면 또는 세포 외 환경에 노출되어 있다. 즉, 미생물 대사체가 ─ 화장품 활성 성분으로서 ─ 도달할 수 있는 자리다. 그리고 이 단백질들의 결합 자리 구조를 알면, 후보 메타볼라이트의 결합 친화도를 in silico로 추정할 수 있다 — wet-lab 검증을 받기 전에. 이것이 Chapter 4가 다룬 "분자 fingerprint 기반 endpoint 점수 예측"보다 한 단계 깊은 모델링이며, AlphaFold가 가능하게 만든 새 층위다.
5.2 AlphaFold2 — 변곡점의 정확한 위치
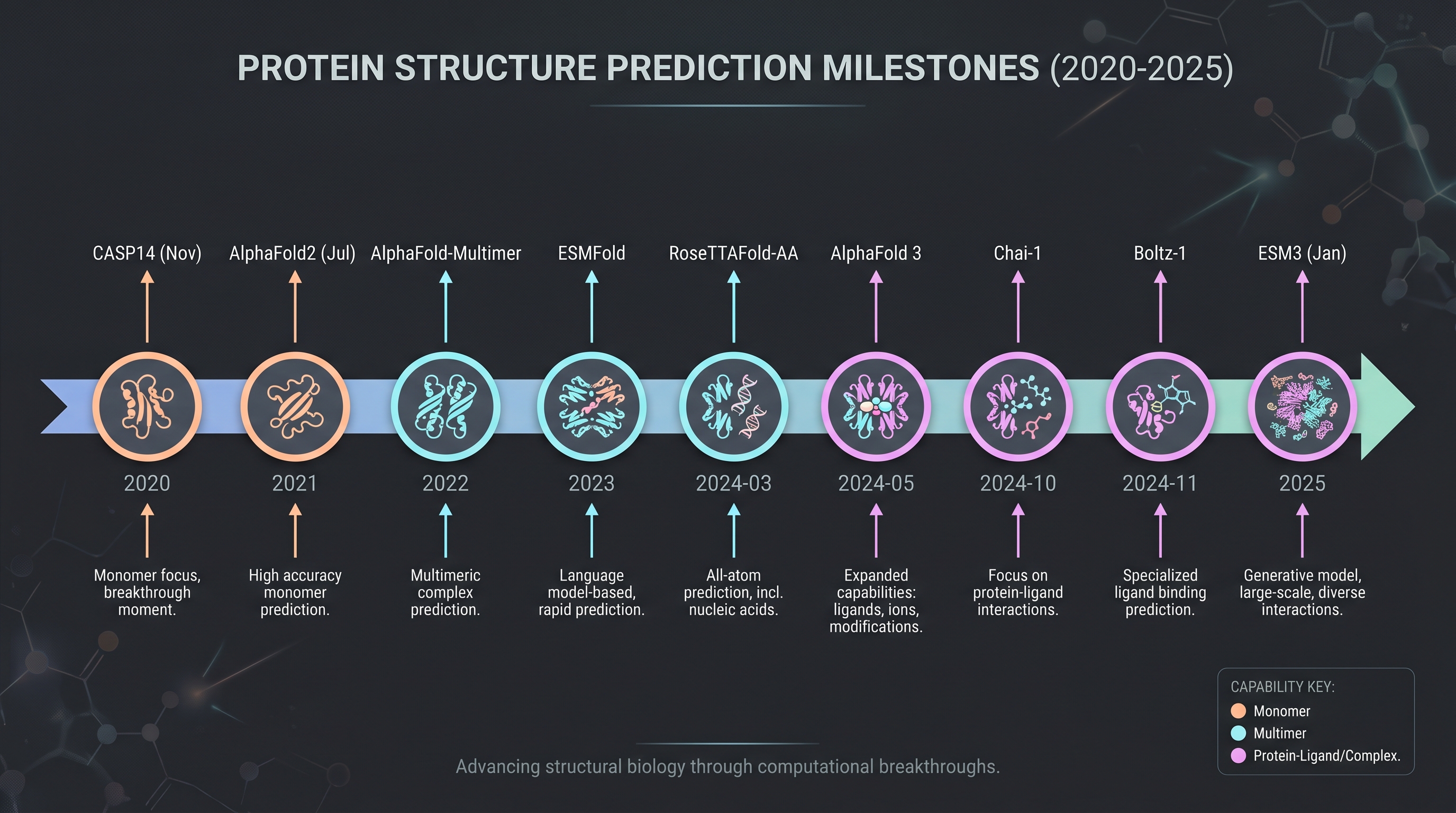
2020년 11월 CASP14(critical assessment of protein structure prediction) 결과 발표는 분야의 분기점이었다. [14]의 DeepMind 그룹이 출품한 AlphaFold2는 평균 GDT-TS 87.0, 중간값 92.4를 기록했다 — 2위 그룹과의 격차가 한 세대 분이었고, X-ray 결정학의 실험 오차에 들어간 첫 계산 모델이었다. 핵심 아키텍처 혁신은 두 가지였다:
- Evoformer: multiple sequence alignment(MSA)와 pair representation을 서로 업데이트하며 진화적·구조적 정보를 동시에 학습. 진화적 공변이(co-evolution)가 가까운 잔기 쌍을 알려주고, 그 가까움이 다시 MSA 해석을 정제한다.
- Structure module: 3D 좌표를 SE(3)-invariant 방식으로 직접 회귀. 잔기 frame(N-Cα-C)을 회전·이동으로 표현하고, IPA(invariant point attention)로 좌표·방향·신뢰도(pLDDT)를 동시에 예측.
발표 4개월 뒤 [14]의 동료 모델인 RoseTTAFold가 출간되며 — David Baker 그룹의 [3] — three-track(서열·거리·좌표) 신경망으로 비슷한 정확도를 GPU 자원의 5분의 1로 재현했다. 이 두 결과의 동시 등장은 우연이 아니다. Evoformer 같은 아키텍처가 한 그룹의 기적이 아니라 분야 전체의 수렴점이었다는 신호다.
산업 즉시 효과: [17]의 ESMFold(Meta AI / EvolutionaryScale)가 2022–2023년 사이 6억 1,700만 개의 메타지노믹 단백질 구조를 ESM Metagenomic Atlas로 공개했다. ESMFold는 MSA 없이 language model embedding만으로 구조를 추정하므로 속도가 AlphaFold2의 60배 — 화장품 R&D 입장에서 "공개된 미생물 메타지노믹 단백질이 거의 다 이미 구조화되어 있다"는 상태가 된 셈이다. iHSMGC의 1,094만 개 피부 마이크로바이옴 유전자(Chapter 3)도 ESMFold 통과 후 거의 모두 좌표를 가지고 있다고 가정해도 무리가 없다.
그러나 AlphaFold2의 한계도 명확했다. (1) 단일 사슬 단량체 위주 — 복합체는 [6]의 AlphaFold-Multimer 확장 이후에야 안정화. (2) 리간드·이온·DNA·RNA는 다루지 못함 — 약물·메타볼라이트 도킹은 별도 도구(AutoDock Vina, GNINA 등)에 의존. (3) 동적 conformation, 알로스테릭 상태, 막관통 단백질의 lipid-protein 상호작용은 잡지 못한다.
세 번째 한계가 화장품에 특히 아프다. 피부 활성 성분의 표적은 MMP 같은 분비 효소뿐만 아니라 GPCR(TRPV1·PAR2)과 인테그린 같은 막관통 수용체가 많다. AlphaFold2의 단일-구조 예측만으로는 ligand-bound active state과 ligand-free inactive state의 구별이 어렵고, lipid bilayer 환경의 영향도 반영되지 않는다. 이 한계는 AlphaFold 3에서 부분적으로만 풀렸다.
5.3 AlphaFold 3 — 메타볼라이트-단백질 복합체를 결정학 없이 예측
2024년 5월 [1]가 Nature에 발표한 AlphaFold 3는 단백질 구조 예측에서 모든 종류의 생체 분자가 함께 있는 시스템의 구조 예측으로 도약했다. 단백질·DNA·RNA·리간드·이온·공유 결합 변형(인산화·당화 등 일부 PTM)을 한 모델 안에서 처리한다. 아키텍처 변화의 핵심은 두 가지:
- Diffusion 기반 좌표 생성: 기존 structure module을 buritto diffusion module로 교체. 노이즈에서 좌표를 점진적으로 정제하는 방식은 RFdiffusion·de novo 단백질 설계 흐름과 같은 패러다임이며, 다양한 분자 타입을 단일 표현으로 다룰 수 있다는 이점이 있다.
- 포괄적 입력 인코딩: 단백질뿐 아니라 small molecule SMILES, 핵산 서열, 이온이 같은 grammar로 들어간다. 사용자 입장에서는 한 번에 "단백질 X + 리간드 Y의 복합체"를 요청할 수 있다.
벤치마크에서 AlphaFold 3는 단백질-리간드 도킹에서 PoseBusters set 76.4%를 통과 — 기존 SOTA AutoDock Vina의 ~52%보다 크게 높다. 단백질-DNA·RNA 복합체에서도 RoseTTAFoldNA보다 우위. 화장품 시사: MMP-1과 미생물 메타볼라이트(예: COSMAX의 [15] spermidine, Cutibacterium가 만드는 단쇄지방산·포르페린)의 결합 자세를 결정학적 동결 구조 없이 예측할 수 있다는 뜻이다. 콜라겐 분해 억제 후보의 IC50을 wet-lab 전에 추정할 수 있는 단계로 진입한 셈이다.
그러나 [1]는 두 가지 한계를 명시한다. (1) 친화도(affinity, ΔG·Kd·IC50)는 직접 예측하지 않는다 — 결합 자세(pose)만 예측. 친화도는 별도 후처리(MM-PBSA, FEP, 또는 ML scoring function)가 필요하다. (2) 상업적·라이선스 제약이 강했다 — 발표 초기에는 DeepMind의 AlphaFold Server를 통한 비상업 비공개 사용만 허용됐다. 2024년 11월 ~ 2025년 초 사이 weights가 비상업 학술용으로 공개되면서 ([1]의 보충 라이선스), 산업 사용은 여전히 그레이 존이었다. 이 라이선스 충돌이 곧 오픈소스 복제 경쟁의 직접적 도화선이 됐다.
5.4 오픈소스 복제 경쟁 — Boltz, Chai, RoseTTAFold-AllAtom, ESM3
AlphaFold 3가 폐쇄형이라는 사실은 학계와 인접 산업에 강한 동기를 줬다. 2024년 한 해 동안 세 개의 오픈 가중치(또는 그에 준하는) 복제·확장 모델이 나왔다.
RoseTTAFold All-Atom ([16], Science, 2024-03). David Baker 그룹의 후속 — three-track 신경망을 모든 원자 표현으로 일반화. 단백질뿐 아니라 핵산·소분자·금속 이온을 다룬다. RFdiffusion과의 자연스러운 결합으로 de novo 단백질 설계까지 한 파이프라인 안에 묶이는 게 강점. 가중치는 비상업 학술용으로 공개. 화장품에서의 의미: collagen-mimic 펩타이드 같은 새로운 단백질을 디자인하여 MMP를 경쟁적으로 저해하는 시나리오까지 가능 — Chapter 7의 합성생물학과 직결된다.
Boltz-1 ([22], MIT Jameel Clinic 기술 보고, 2024-11). AlphaFold 3에 가장 가까운 오픈 가중치 복제. MIT Jameel Clinic이 OpenAlphaFold-3 이니셔티브로 11월 19일에 공개. MIT 라이선스로 상업 사용 가능한 점이 결정적이며, 화장품·바이오 산업이 가중치를 다운로드해 사내에서 미세조정·재배포할 수 있는 첫 본격 모델이 됐다. 정확도는 AlphaFold 3 대비 PoseBusters에서 1~5% 정도 낮지만, 라이선스 자유도가 그 차이를 상쇄한다 — 산업 도입의 임계점이 곧 라이선스라는 점을 보여준 사례다.
Chai-1 ([4], 2024-10). Chai Discovery 스타트업(Glen Weyl 등이 자문)이 발표한 또 다른 AlphaFold 3 동급 모델. 비상업 학술용 가중치 + 상업용 API. AlphaFold 3와 비교한 자체 벤치마크에서 protein-ligand pose 정확도에서 동등하거나 일부 셋에서 우위를 주장. 라이선스 모델이 SaaS형이라 화장품 R&D 입장에서는 Boltz와 다른 트레이드오프 — 자체 운영 부담은 없지만 데이터·결과가 외부로 흐른다.
ESM3 ([12], Science, 2025-01). EvolutionaryScale의 단백질 언어 모델. 98B 파라미터 — 7B 모델은 오픈 — 로 단백질 서열·구조·기능을 한 토큰 스트림으로 통합 학습한다. ESMFold(2022–2023)의 진화판이지만 구조 외에 기능·서열도 함께 생성할 수 있다 — 즉, "특정 결합 자리에 맞는 새로운 단백질 서열을 만들어 줘"가 가능하다. EvolutionaryScale는 2024년 6월 [7]의 1억 4,200만 달러 시드와 AWS·NVIDIA 인프라 파트너십과 함께 출범했으며, ESM3는 화장품·합성생물학 입장에서 가장 직접 적용 가능한 도구다. Chapter 7의 비건 콜라겐(Modern Meadow/Evonik Vecollage [8], Geltor PrimaColl [9])이 이런 도구로 디자인된 단백질의 첫 산업화 사례다.
이 네 모델의 동시 등장이 의미하는 바는 단순하다 — AlphaFold 3-class 도구는 2024년 말 기준 commodity다. 라이선스 선택(폐쇄형 SaaS·오픈 학술·상업 가능 오픈)만 다를 뿐 정확도 차이는 1~5% 수준. 화장품 R&D 입장에서 "가중치 접근권"이 더 이상 진입 장벽이 아니라는 사실이 핵심이다.
[2]의 Bioinformatics Advances 도구는 이 흐름에 응답한다 — AlphaFold 3·Boltz-1·Chai-1을 같은 입력으로 돌려 결과를 정량 비교하는 워크플로우를 제공한다. 산업 도입 표준이 곧 "한 모델만 쓰지 말고 세 모델을 다 돌려 일치도(consensus)를 본다"로 굳어지고 있는 신호다.
5.5 화장품 타겟 도킹 파이프라인 — 구체적 예
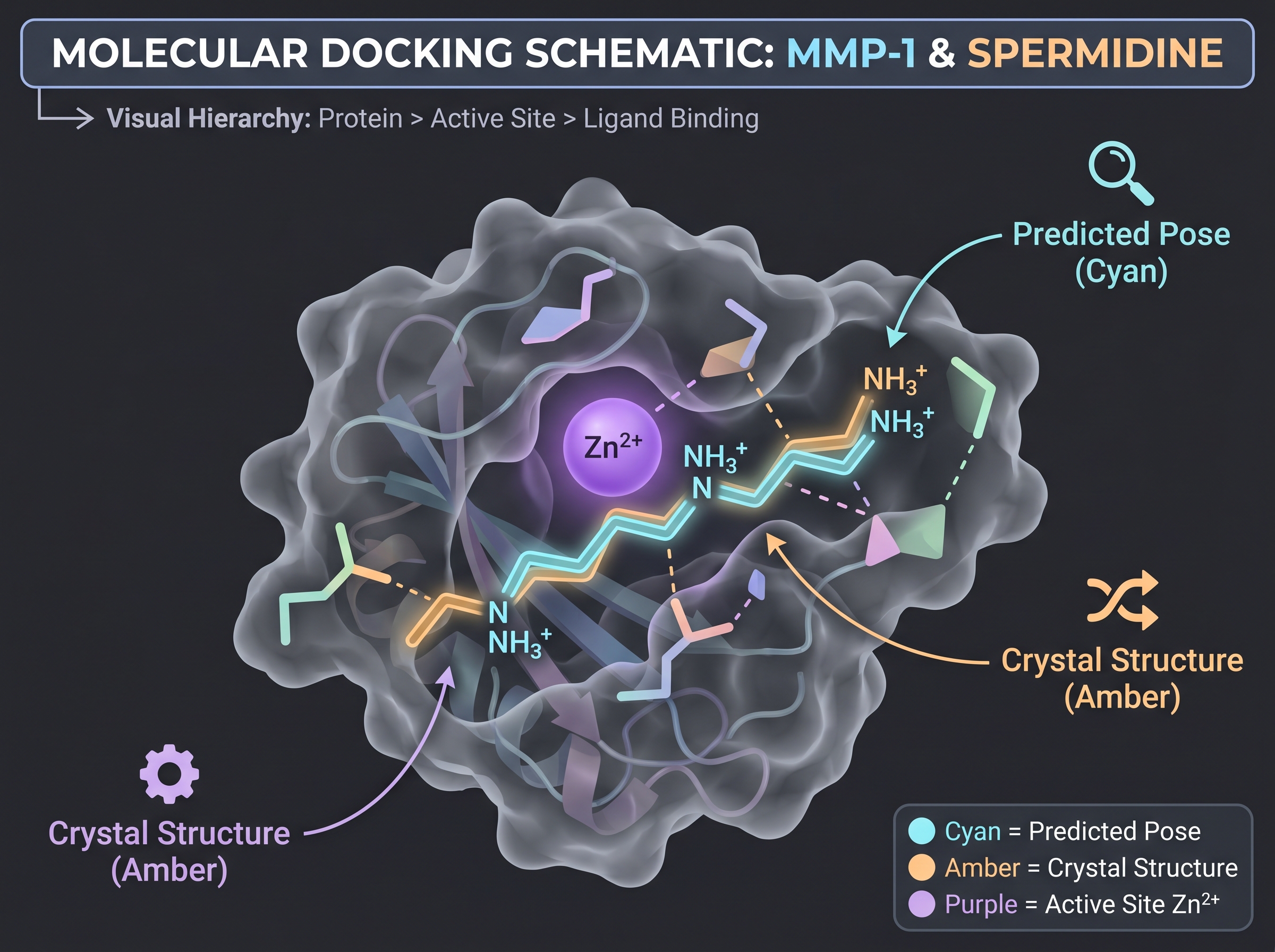
이 챕터의 추상을 구체화하기 위해, 마이크로바이옴 메타볼라이트 한 분자를 예로 들어 전체 파이프라인을 따라가보자. 사례는 COSMAX/Dankook 그룹의 [15]가 Communications Biology에 발표한 spermidine (피부 미생물 대사체 — Lactobacillus 등이 생산하는 폴리아민)이다.
1단계 — 구조 정보 확보.
- spermidine은 small molecule이므로 SMILES
NCCCCNCCCN로 표현. ChEMBL·PubChem에서 즉시 검색 가능. - 피부 단백질 표적 후보: MMP-1, MMP-9 (콜라겐 분해), TGM3 (transglutaminase, 각질 가교), AHR. In vitro에서 [15]가 fibroblast collagen recovery를 확인했으므로 콜라겐 합성·분해 축이 가장 그럴듯하다.
- MMP-1 구조: PDB ID 1HFC, X-ray 1.56Å 분해능. AlphaFold DB에도 UniProt P03956 entry로 등록.
2단계 — 도킹.
- AlphaFold 3 또는 Boltz-1에 "MMP-1 (UniProt P03956) + spermidine (SMILES)"을 입력. 출력은 결합 자세(pose) + per-residue confidence(pLDDT). 핵심 결과: spermidine이 MMP-1의 zinc-binding 활성 자리 근방에 결합하는지, 아니면 알로스테릭 자리에 결합하는지.
- 비교군: 같은 입력을 AutoDock Vina에 넣은 baseline 점수. AlphaFold 3-class 도구의 결합 자세는 일반적으로 Vina 대비 RMSD 1~2Å 이내로 더 정확하다([1] 본문 Figure 4).
3단계 — 친화도 추정.
- AlphaFold 3·Boltz-1은 pose만 주고 ΔG는 직접 주지 않는다. 후처리로 MM-GBSA·MM-PBSA를 돌려 ΔG를 추정 — 약 ±2 kcal/mol 오차로 IC50 자릿수까지는 잡힌다.
- 또는 ML scoring function(GNINA, DiffDock-L 등) 사용.
- 결과 예시: 추정 IC50 50–200 μM 자리 — wet-lab 확인이 필요한 범위.
4단계 — wet-lab 검증 (Chapter 3의 "AI 예측, 배양 검증" 명제).
- MMP-1 효소 활성 assay(EnzChek, fluorogenic substrate)에서 spermidine의 IC50 측정.
- Primary fibroblast에서 procollagen ELISA, MMP-1 western blot.
- 일치 여부 확인 — AlphaFold 3 예측 IC50과 in vitro IC50이 같은 자릿수에 떨어지면 후보 통과. 차이가 10배 이상이면 결합 자리 재검토.
5단계 — 데이터 축적과 다음 후보로의 일반화.
- 검증된 pose는 사내 학습 데이터로 쌓인다. 후속 후보(Cutibacterium의 단쇄지방산, Staphylococcus epidermidis의 epifadin 펩타이드 등)의 도킹 파이프라인에 prior로 들어간다.
이 5단계 파이프라인은 이미 [13]가 IPF 표적(TNIK 키나아제)에 대해 임상 2a까지 가져간 흐름과 동일하다 — 차이는 cosmetic endpoint vs drug endpoint, 그리고 산업 인센티브뿐이다.
5.6 한계와 빈 구멍
도구가 commodity여도 화장품 도메인 적용에서 막히는 자리는 여전히 많다. 정직한 매핑은 다음과 같다.
5.6.1 친화도 정량은 자세 예측보다 훨씬 어렵다.
[1]의 명시적 한계 — AlphaFold 3-class 모델은 결합 자세는 잘 예측하지만 친화도는 직접 예측하지 않는다. 도킹 후 ΔG 추정에 쓰이는 MM-PBSA·FEP·ML scoring function은 각각 단점이 있고, 일반적으로 ±2 kcal/mol 오차 — 즉, IC50 한 자릿수 정도의 불확실성이 남는다. 화장품 R&D 입장에서 "IC50 50 μM" vs "IC50 500 μM"의 차이는 제품 개발 가능 여부를 가른다 — 결합 자세만으로는 그 선을 그을 수 없다.
5.6.2 PTM이 화장품 타겟에서 매우 흔하다.
피부 표적 단백질의 상당수는 당화(N-glycosylation)·인산화·황화 등 post-translational modification을 갖는다. MMP-9의 활성 조절은 인산화에 의존하며, 점막·표피 단백질(필라그린, 인볼루크린)은 광범위한 당화 패턴을 가진다. AlphaFold 3는 일부 PTM을 명시적으로 다루지만 전부는 아니며, 특히 화장품 R&D에 중요한 복잡한 당화 사슬 모델링은 여전히 제한적이다. [1] supplementary에서 명시.
5.6.3 막관통 수용체 — GPCR과 인테그린.
화장품의 sensing 타겟(TLR2, TRPV1, PAR2, integrins αVβ3 등)은 대부분 막관통이다. AlphaFold-class 모델은 lipid bilayer 환경을 명시적으로 모델링하지 않으며, GPCR의 active vs inactive conformation 구별이 정확도가 낮다. [16]의 RoseTTAFold-AllAtom과 ESM3가 일부 개선했지만, 막관통 표적에서의 ligand pose 예측은 여전히 cytosolic 단백질 대비 정확도가 떨어진다. 결과적으로 GPCR 표적 화장품 R&D는 도킹 결과를 더 보수적으로 해석해야 한다.
5.6.4 동적 conformation과 알로스테릭 자리.
단일 정적 구조만으로는 conformational ensemble을 잡지 못한다. MMP-3 같은 효소는 open 과 closed 상태를 오가며, 각각의 결합 친화도가 다르다. molecular dynamics 시뮬레이션(GROMACS, OpenMM)을 후처리로 돌리거나, AlphaFold-multimer를 alternative MSA로 돌려 ensemble을 강제로 생성하는 우회 방법이 쓰이지만, 표준 워크플로우는 아직 합의가 없다.
5.6.5 검증 데이터의 부재(Gap 1).
[11]의 PRISMA 종설(74편)은 AI 디자인된 화장품 활성 성분의 동료 심사 임상 readout이 0건이라고 명시한다. AI 도구는 commodity여도, 산업이 그 도구로 만든 활성 성분의 임상 검증된 사례를 발표하지 않으면 모델의 외부 신뢰성(external validity)은 검증되지 않는다 — 이것이 학술 비교 가능성에서 화장품이 제약에 뒤처지는 직접적 원인이다.
5.7 기회의 빈자리 — Insilico의 readout이 화장품에도 와야 한다
[11]의 명시: 2026년 5월 현재, AI 도구로 디자인된 화장품 활성 성분이 동료 심사 임상 결과를 낸 사례는 없다. 가장 가까운 인접 산업 readout은 [13]의 Nature Medicine — rentosertib(TNIK 억제제, 특발성 폐섬유증 IPF) 임상 2a에서 12주 +98.4 mL FVC vs 위약 −20.3 mL의 효능 readout. [19]의 Nature Biotechnology 동반 논문은 표적 발굴(PandaOmics)부터 IND 제출까지 30개월이 걸렸다고 명시한다 — 전통적 신약 발굴의 6~8년 대비 압도적.
화장품 산업이 빌릴 수 있는 템플릿:
- 표적 발굴 단계의 AI — 피부 노화의 인과 단백질 (PandaOmics 같은 multi-omics target ID + AlphaFold 구조 가용성 필터).
- 분자 디자인 — generative chemistry (Chemistry42, Cradle [5], Profluent [20]) + AlphaFold 3-class 도킹 검증.
- 합성·검증의 압축 — 합성생물학 균주(Chapter 7) + ex vivo 피부 모델(Chapter 9).
- 임상 readout 발표 — Insilico가 Nature Biotechnology와 Nature Medicine 양쪽에 발표한 패턴은 산업 신뢰 구축의 표준이 됐다. 화장품도 동일 채널(JAAD, British Journal of Dermatology, Skin Pharmacology and Physiology)에서 readout을 발표하면 카테고리 정의 자산이 된다.
가장 그럴듯한 첫 발표 후보: 한국 산업(COSMAX, Amorepacific, LG H&H 중 한 곳) 또는 EU 중견(Lactobio·S-Biomedic 등 microbiome 특화 회사). 미국 빅5(L'Oréal, Unilever, Estée Lauder, P&G, Shiseido)는 마케팅 ROI상 동료 심사보다 보도 자료를 우선할 가능성이 높다. 자세한 산업 매핑은 Chapter 10·Chapter 11에서.
비건 콜라겐은 이미 첫 발걸음을 뗐다. [9]의 PrimaColl(생분해성 비건 콜라겐)은 2025년 10월 FDA GRAS "no questions" letter를 받았으며, [8]의 Vecollage Fortify L(Modern Meadow와 협업)은 화장품 등급 비건 콜라겐의 첫 상업화. 둘 다 단백질 디자인 단계에서 ESM3·RoseTTAFold-AllAtom 계열 도구를 활용한 것으로 알려져 있다 — 단 직접적인 동료 심사 readout(임상)은 아직 없고, GRAS letter나 press 채널 발표에 머문다.
5.8 Open Questions
- 친화도 예측의 단계 변화 — 현재 ±2 kcal/mol 오차의 한계가 어떤 데이터·아키텍처 조합으로 ±0.5 kcal/mol 수준까지 떨어질 것인가? FEP+ML scoring의 결합이 단기 가장 그럴듯한 답이지만, 화장품 도메인의 친화도 데이터는 ChEMBL 같은 약학 데이터보다 훨씬 sparse하다.
- 막관통 수용체의 격차 해소 — GPCR active/inactive conformation 구별과 lipid-protein 상호작용 모델링은 AlphaFold 3-class 도구의 일관된 약점이다. 화장품 sensing 타겟이 다수 GPCR이라는 점에서 이 격차는 직접 비즈니스 영향. 어떤 도구·데이터가 격차를 좁힐 것인가?
- 시뮬레이션-검증 사이클의 비용 구조 — 도킹 한 번이 GPU 분 단위로 떨어졌지만 wet-lab MIC·IC50 검증은 여전히 후보당 수십~수백 달러. 이 비대칭이 화장품 R&D 조직의 병목을 어디로 옮기는가? Chapter 9에서 이 질문을 임상 단계까지 끌어 확장한다.
- PTM의 in silico 처리 — 화장품 타겟에 흔한 복잡한 당화·황화의 모델링은 AlphaFold 3에서도 제한적이다. 향후 어떤 도구가 이 격차를 채울 것인가? RoseTTAFold-AllAtom과 GLYCAM 계열 sugar-binding 도구의 결합이 가능성.
- 데이터 비대칭의 함의 — 화장품 R&D가 도킹 결과를 발표하지 않는 한, 모델의 external validity는 제약 산업 readout에 의존한다. 이 의존 구조가 화장품 도구 선택과 검증 표준에 어떤 영향을 미치는가? Chapter 12에서 통합 결론.
참고문헌
- Abramson, J., Adler, J., Dunger, J. et al. (2024). Accurate structure prediction of biomolecular interactions with AlphaFold 3. Nature 630, 493–500.
- ABCFold authors (2025). ABCFold: easier running and comparison of AlphaFold 3, Boltz-1, and Chai-1. Bioinformatics Advances 5(1):vbaf153. [Abcfold, 2025]
- Baek, M., DiMaio, F., Anishchenko, I. et al. (2021). Accurate prediction of protein structures and interactions using a three-track neural network. Science 373(6557):871–876.
- Chai Discovery Team (2024). Chai-1: Decoding the Molecular Interactions of Life. bioRxiv 2024.10.10.615955; Chai Discovery technical report. [Chai Discovery, 2024]
- Cradle Bio (2024). Cradle AI protein design platform — $73M Series B. TechCrunch / SynBioBeta, Nov 2024. [Cradle, 2024]
- Evans, R., O'Neill, M., Pritzel, A. et al. (2022). Protein complex prediction with AlphaFold-Multimer. bioRxiv 2021.10.04.463034.
- EvolutionaryScale (2024). EvolutionaryScale launch with ESM3 — $142M seed and commercial protein-design platform. Press release, June 25, 2024. [EvolutionaryScale, 2024]
- Evonik (2024). Evonik Vecollage Fortify L — vegan collagen for cosmetic personal care (Modern Meadow partnership). Evonik press, Feb 2024. [Evonik, 2024]
- Geltor (2025). Geltor PrimaColl — first FDA GRAS letter for biodesigned vegan collagen. FoodNavigator-USA / SynBioBeta / Geltor press, Oct 2025. [Geltor, 2025]
- Hashimoto, K., Yamamoto, T., Yagi, M. et al. (2022). NRF2 activation by Galactomyces ferment filtrate complements the AHR-axis mechanism in skin barrier homeostasis. Journal of Cosmetic Dermatology, 2022. [Hashimoto et al., 2022]
- Haykal, D., Flament, F., Amar, D. et al. (2025). Cosmetogenomics unveiled: a systematic review of AI, genomics, and the future of personalized skincare. Frontiers in Artificial Intelligence 8:1660356.
- Hayes, T., Rao, R., Akin, H. et al. (2025). Simulating 500 million years of evolution with a language model (ESM3). Science, Jan 2025.
- Insilico Medicine clinical authors, Ren, F., Zhavoronkov, A. et al. (2025). A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine, May 2025. [Insilico, 2025]
- Jumper, J., Evans, R., Pritzel, A. et al. (2021). Highly accurate protein structure prediction with AlphaFold. Nature 596, 583–589.
- Kim, G., Kim, M., Kim, M. et al. (2021). Spermidine-induced recovery of human dermal structure and barrier function by skin microbiome. Communications Biology 4:231.
- Krishna, R., Wang, J., Ahern, W. et al. (2024). Generalized biomolecular modeling and design with RoseTTAFold All-Atom. Science 384:eadl2528.
- Lin, Z., Akin, H., Rao, R. et al. (2023). Evolutionary-scale prediction of atomic-level protein structure with a language model (ESMFold + ESM Metagenomic Atlas). Science 379:1123–1130.
- Novo Nordisk; Cradle (2024). Novo Nordisk × Cradle AI protein design partnership disclosure. Cradle Series B + Novo press, 2024. [Novo Nordisk, 2024]
- Ren, F., Ding, X., Zheng, M. et al. (2024). A small-molecule TNIK inhibitor (ISM001-055 / rentosertib) discovered via end-to-end generative AI from target identification to Phase 1. Nature Biotechnology, Mar 2024.
- Ruffolo, J. A., Nayfach, S., Gallagher, J. et al. (2024). Design of highly functional genome editors by modeling the universe of CRISPR-Cas proteins (Profluent ProGen2 / OpenCRISPR-1). bioRxiv 2024.04.22.590591.
- Takei, K., Mitoma, C., Hashimoto-Hachiya, A. et al. (2015). Galactomyces ferment filtrate as AHR agonist restoring filaggrin and skin barrier function. Journal of Dermatological Science, 2015. [Takei et al., 2015]
- Wohlwend, J., Corso, G., Passaro, S. et al. (2024). Boltz-1: Democratizing Biomolecular Interaction Modeling. bioRxiv 2024.11.19.624167; MIT Jameel Clinic technical report.