Chapter 1: 화장품 속 미생물 — 발효 화장품의 역사와 한계
1.1 왜 이 챕터를 읽는가 — "발효 화장품"이라는 단어가 두 번 바뀐다
화장품 매장 카운터에서 "발효(ferment)"라는 단어는 1980년대에 한 번, 그리고 2010년대 중반에 또 한 번 의미가 바뀌었다. 첫 번째 변화는 사케 양조장 옆에 서 있던 한 일본 기술자가 효모로 발효시킨 액체가 양조공 손바닥을 매끈하게 만든다는 관찰에서 시작되어, 1980년 SK-II Pitera라는 단일 발효 여과액 제품으로 상품화되었다. 두 번째 변화는 그 발효액의 작용 기전이 분자 수준에서 처음 설명된 [17]의 AHR(aryl hydrocarbon receptor) 논문이 Clinical and Experimental Dermatology에 실린 시점에 일어났다 — 제품 출시로부터 35년이 지난 뒤였다.
이 35년의 간극이 이 챕터의 주제다. 마이크로바이옴 화장품이 무엇이고 왜 지금 AI가 변곡점이 되었는지 이해하려면, 그 전에 발효 화장품 1세대가 무엇을 했고 무엇을 모른 채 했는지를 정직하게 정리해야 한다. 마케팅 언어로 30년을 살아남은 카테고리가 메타지노믹스·AI·합성생물학이라는 데이터 중심 도구에 의해 어떻게 다시 쓰이고 있는지가 책 전체의 출발점이다.
이 챕터는 비전문가 독자(화장품 기획자·기자·투자자)를 가정한다. 분자생물학 사전 지식 없이 따라올 수 있게 쓰되, 후속 챕터(Chapter 3·Chapter 5)가 의지할 핵심 개념과 미해결 질문은 명시적으로 남긴다.
이 챕터의 정량적 핵심 3가지
- 35년 — 산업 출시(1980, SK-II Pitera)와 분자 기전 첫 규명([17]) 사이의 간극.
- 약 1,000배 — 인간 게놈 1개 시퀀싱 비용이 2005년 약 1,000만 달러에서 2014년 약 1,000달러로 떨어진 폭 (US NHGRI Cost-per-Genome data). 이 곡선이 무너지지 않았다면 피부 마이크로바이옴 atlas는 존재할 수 없었다.
- 205편 — 2025년 한 해에 Cosmetics 한 저널에만 게재된 마이크로바이옴·바이오엔지니어드 화장품 관련 논문/리뷰의 누적 인덱싱 수 (예: [1]가 권호 마지막 issue로 발행).
1.2 1세대 발효 화장품 — 무엇을 했고, 무엇은 우연이었는가
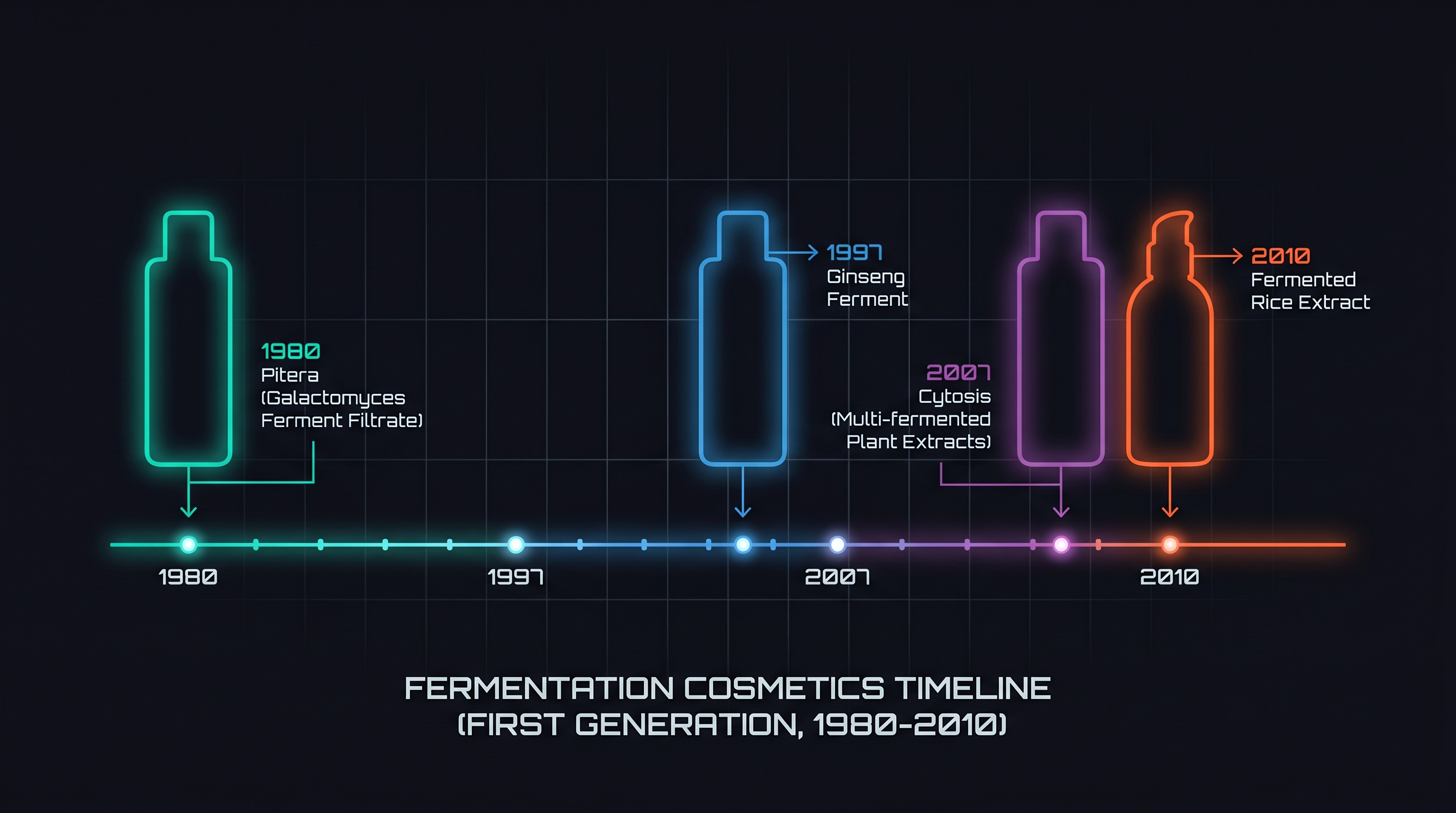
발효 화장품 1세대는 세 가지 경험적 관찰에 기대 구축됐다.
관찰 1 — 발효 여과액(ferment filtrate)에는 항노화·진정 효과가 있더라. SK-II Pitera는 Galactomyces(혹은 Pichia) 효모를 청주 양조 공정에서 거른 액체에서 출발했다. 1990년대 일본·한국 시장에서 동의보감·한방 처방을 효모·유산균으로 발효시킨 한국형 발효 화장품군이 잇따라 출시되었고, 2010년 전후 SUM37·헤라·후·설화수의 발효 라인이 1조 원대 매출 카테고리를 형성했다.
관찰 2 — Lactobacillus·Bifida·Saccharomyces 발효 여과액에는 임상에서 측정 가능한 보습·진정 신호가 있더라. 이 신호는 2000년대 초중반 in vitro 케라티노사이트(keratinocyte) 어세이와 12주 임상 시험에서 부분적으로 확인되었다. 단, 거의 모든 실험은 단일 균주의 발효물 vs 위약 구도였다 — "발효 산물 안의 어떤 분자가 어떤 수용체에 결합해 어떤 유전자를 켜는가"는 답하지 않았다.
관찰 3 — 균주 자체보다 발효 산물(fermentate)이 더 안전하다더라. 살아 있는 균을 화장품에 넣으면 보존계·안정성·규제 문제가 폭증하므로, 사실상 모든 1세대 발효 화장품은 균을 죽이거나 여과액(filtrate)만 추출한 포스트바이오틱(postbiotic) 형태였다. 이 결정은 분자생물학적 통찰이 아니라 산업 운영의 제약에서 나왔다.
이 세 관찰을 한 줄로 요약하면 이렇다 — 1세대는 "효과가 있는 듯하다"는 결과(empirical efficacy)에는 도달했지만, "왜 효과가 있는가"라는 메커니즘(mechanism)에는 도달하지 못했다. [12]의 프로바이오틱 비판적 리뷰는 이 mechanism-deficit이 비단 화장품 산업의 문제가 아니라 프로바이오틱 산업 전반의 구조적 결함이었음을 지적한다.
1.2.1 Galactomyces — 35년 만에 채워진 메커니즘 공백
가장 유명한 1세대 발효물의 분자 기전이 채워진 것은 [17]가 처음이었다. 이 논문은 Galactomyces ferment filtrate(GFF)가 케라티노사이트의 AHR(aryl hydrocarbon receptor)을 활성화하여, Th2 사이토카인(IL-4·IL-13)에 의해 억제된 filaggrin 발현을 회복시킨다는 메커니즘을 처음으로 분자 수준에서 보였다. AHR은 트립토판 대사산물·미생물 대사체에 반응하는 핵 수용체이고, filaggrin은 피부 장벽의 핵심 단백질이다.
[7]는 7년 뒤 같은 Galactomyces 추출물이 NRF2(nuclear factor erythroid 2-related factor 2) 경로를 통해 항산화 반응(HO-1·NQO1)을 켜고, NF-κB 매개 염증 신호를 억제한다는 두 번째 분자 축을 추가했다. AHR + NRF2 — 두 축이 함께 묶이며 비로소 "왜 1980년대 양조공의 손이 매끈했는가"가 분자 수준에서 해석되었다.
이 사례는 두 가지를 시사한다. 첫째, 경험적 효능은 거짓이 아니었다 — 단지 설명이 늦었을 뿐이다. 둘째, 분자 기전이 밝혀지기까지 35년이 걸린 이유는 AHR이라는 수용체가 1990년대 후반에야 피부 생물학 문맥에서 주류 도구가 되었기 때문이고, 이 시간을 압축하는 도구가 곧 Chapter 5에서 다룰 AlphaFold·ESMFold 같은 단백질 구조 예측이다. 발효 화장품의 "왜?"를 채우는 데 35년이 걸렸다면, AI 시대의 새로운 발효 후보 분자에는 35주가 걸리는 미래가 가능한가 — 이 질문이 Part II 전체의 문제 설정이다.
1.2.2 마케팅 언어와 과학 언어의 비대칭
1세대 발효 화장품의 두 번째 유산은 언어의 비대칭이다. 광고는 "100가지 효능", "황실 비방", "1억 효모 활성"이라는 인상적 표현으로 30년을 살았지만, 같은 기간 peer-reviewed 학술 논문은 다섯 손가락 안에 들었다. [1]는 2025년 시점의 리뷰에서 이 간극을 명시적으로 짚는다 — "대부분의 바이오엔지니어드 활성 성분 효능 주장은 회사 보도자료에 의존하며 peer-reviewed 임상 시험으로 뒷받침되지 않는다."
이 언어 비대칭은 단순히 윤리적 문제가 아니라 데이터 기반 차세대 화장품으로 넘어가는 구조적 장애물이다. 1세대의 모호한 효능 언어를 그대로 두면, 메타지노믹스·AI가 만들어낸 정밀한 endpoint(예: 균주 단위 콜라겐 합성 자극, 부위별 dysbiosis 회복률)도 같은 모호함의 함정에 빠진다. Chapter 8(AI 제형 설계)과 Chapter 12(연구 청사진)가 이 문제를 직접 다룬다.
1.3 시퀀싱 비용 곡선 — 1세대를 끝낸 기술적 변곡점
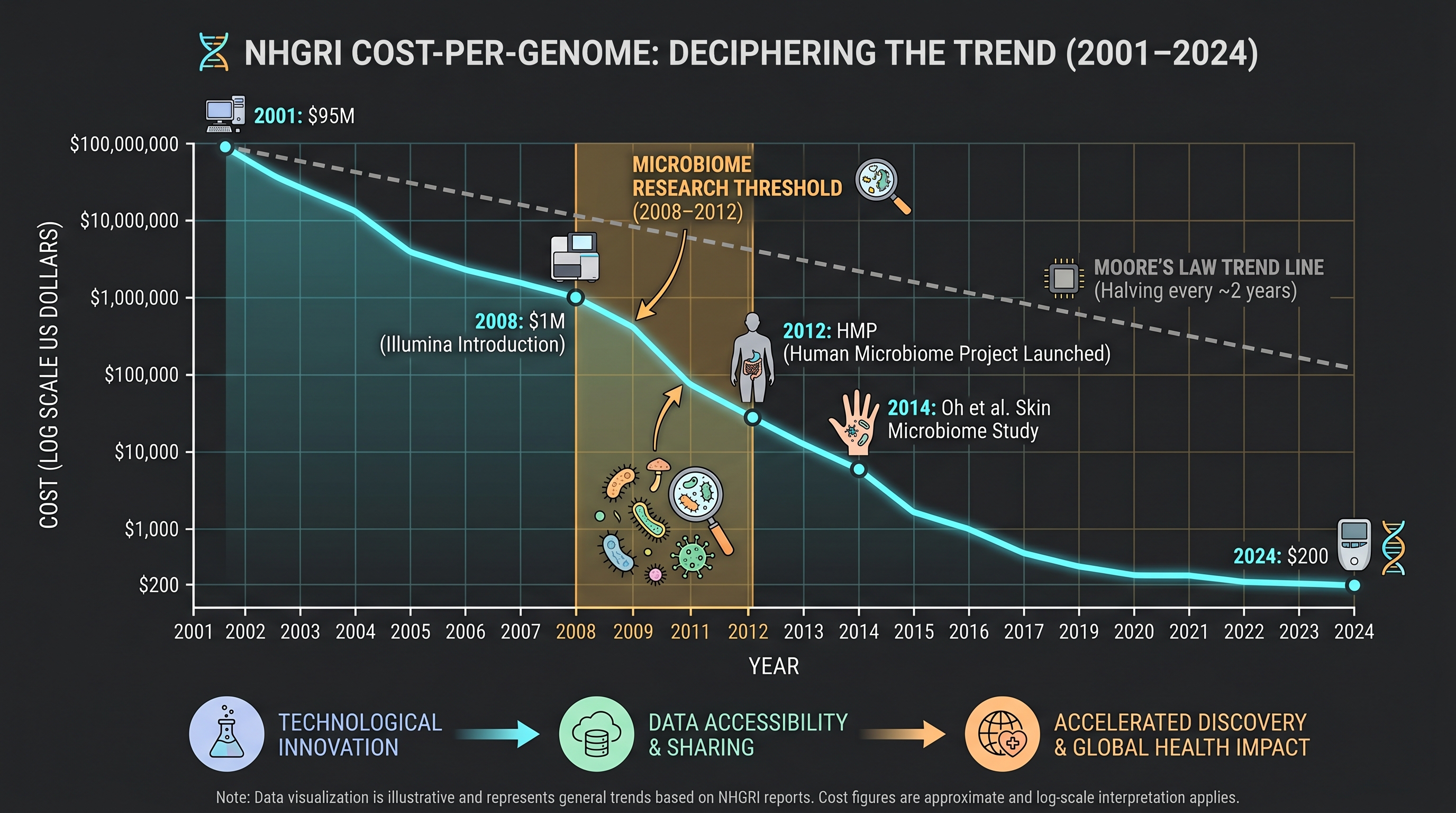
발효 화장품 1세대가 단일 균주·발효 여과액에 머문 가장 큰 외부 제약은 시퀀싱 비용이었다. 2001년 휴먼 게놈 프로젝트 완료 시점의 한 게놈 시퀀싱 비용은 약 1억 달러였다. 2005년 차세대 시퀀싱(NGS, 특히 454/Roche pyrosequencing) 도입 후 비용은 약 1,000만 달러로 떨어졌고, 2014년 Illumina HiSeq X Ten 등장으로 약 1,000달러까지 내려갔다 (US NIH National Human Genome Research Institute의 Cost-per-Genome 추적 데이터).
이 곡선이 어떤 의미였는지를 마이크로바이옴 시각에서 풀어쓰면 이렇다 — 1세대 발효 화장품 기획자에게는 한 사람의 피부에 어떤 균종이 살고 있는지 광범위하게 본다는 옵션 자체가 비용 구조상 존재하지 않았다. 한 사람의 피부 한 부위에서 16S rRNA gene amplicon만 뽑아 군집 구조를 보는 데도 2008년 기준 수천 달러가 필요했고, shotgun metagenomics는 한 자릿수 환자 코호트조차 사치였다. 이 비용 구조가 무너졌을 때 비로소 "피부 전체 생태계"를 본다는 발상이 가능해졌다.
1.4 마이크로바이옴 시대를 연 세 편의 논문 (2009–2012)
비용 곡선이 무너진 직후, 인간 마이크로바이옴 연구는 단 4년 사이에 세 편의 정초 논문으로 골격을 갖춘다.
[2] — Science. Rob Knight 그룹은 9명의 건강한 성인에서 27개 신체 부위의 16S rRNA 시퀀싱을 시간에 따라 반복 수행했다. 결론은 단순하지만 강력했다 — 신체 부위(body site)가 개인차(inter-individual variation)보다 군집 구조를 더 강하게 결정한다. 같은 사람의 손바닥과 입안은 다른 사람의 손바닥끼리보다 훨씬 더 다르다. 이 발견은 "균종 하나를 넣는다"는 1세대 발상이 왜 부분적으로만 작동했는지에 대한 첫 답이었다 — 부위가 다르면 생태계가 다르고, 생태계가 다르면 같은 균이 다르게 행동한다.
[5] — Science. Julia Segre 그룹은 같은 해 Science에 피부 마이크로바이옴 atlas의 정전이 되는 논문을 게재했다. 20개 피부 부위를 sebaceous(피지 분비)·moist(습)·dry(건)의 세 미세환경(microenvironment)으로 나누고, 각 환경의 우점종이 다르다는 것을 보였다 — sebaceous에는 Propionibacterium(현 Cutibacterium)이, moist에는 Staphylococcus·Corynebacterium이, dry에는 더 다양한 community가. 1세대 발효 화장품이 "얼굴 전용" / "바디 전용"으로 구분한 것은 마케팅이었지만, 우연히도 미세환경 구분과 부분적으로 일치했다. 이제 그 구분은 데이터로 정당화될 수 있게 되었다.
[8] — Nature. NIH가 1억 7천만 달러를 투입한 HMP가 5년 만에 첫 reference dataset을 공개했다. 242명의 건강한 성인, 15-18개 신체 부위, 16S rRNA + shotgun metagenomics. 이 데이터는 그 자체로 화장품 산업에 직접 쓰이지는 않았지만, "건강한 피부의 균총이란 무엇인가"라는 reference baseline을 처음으로 인구 규모에서 제공했다. dysbiosis(이상 균총)를 정의하려면 먼저 "정상"을 정의해야 했고, HMP가 그 작업을 했다.
이 세 편은 함께 묶일 때 의미가 완성된다. [6]은 Nature Reviews Microbiology에 발표한 종합 리뷰에서 이 세 논문 이후 5년 사이에 피부 마이크로바이옴 연구가 어떻게 "측정 도구를 갖춘 학문 분야"로 전환되었는지 정리한다 — 비유하자면, 현미경을 갖추기 전과 후의 미생물학 차이다.
1.4.1 곰팡이·균주 해상도·시간 안정성 — 보조 골격을 깐 후속 논문들
세 편의 정초 논문 직후 2013–2016년 사이에 세 가지 보조 골격이 깔렸다.
[3]은 Nature에 ITS(internal transcribed spacer) 시퀀싱을 적용하여 피부 곰팡이 군집 — 특히 Malassezia 속의 부위별 분포 — 을 처음 매핑했다. 발효 화장품이 효모를 다루면서도 정작 피부에 사는 효모 생태계는 까맣게 모른 채 30년을 보냈다는 사실은, 이 시기에야 비로소 인식 가능해졌다.
[4]은 Cutibacterium acnes(당시 Propionibacterium acnes) 안에 RT4·RT5·RT6 등의 ribotype이 존재하며, 같은 종이라도 ribotype에 따라 여드름 병원성이 다르다는 것을 보였다. 종(species) 단위가 아니라 균주(strain) 단위에서 봐야 효능이 보인다 — 이 메시지는 Chapter 2와 Chapter 4가 본격적으로 이어받는다.
[14]의 NIH/Segre lab 연속 작업은 한 개인의 피부 메타게놈이 1–2년에 걸쳐 놀랍게 안정적임을 입증했다. 이는 1세대 발효 화장품의 "균총을 균형 잡아준다"는 광고 언어에 처음으로 정량적 제약을 부과했다 — 균총이 본래 안정적이라면, 한 병의 화장품이 7일 안에 그것을 "리셋"할 수 있다는 주장은 증거 부담이 매우 높다.
1.5 AI를 위한 무대 — AlphaFold 직전까지의 ML for biology
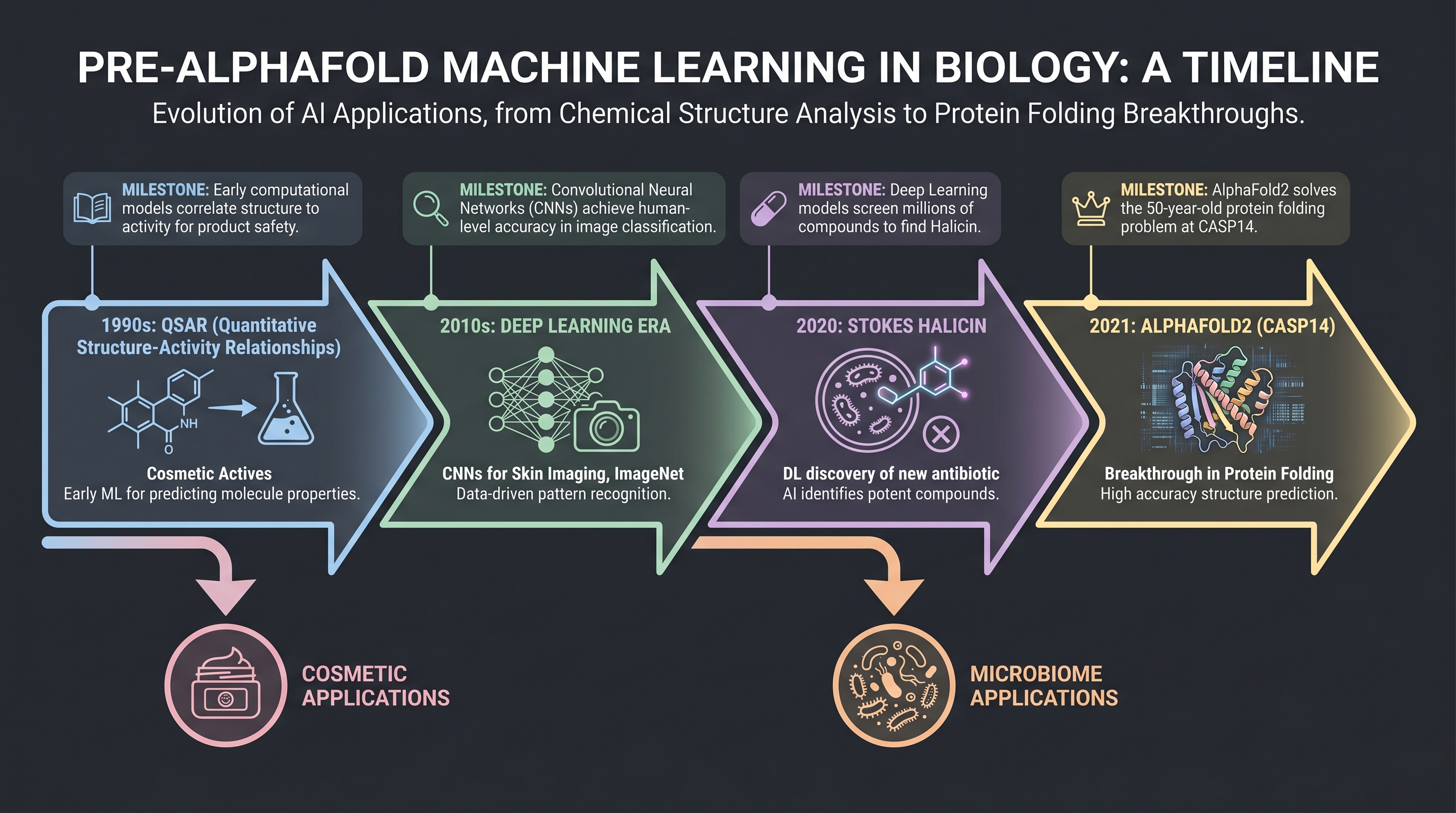
이 책의 핵심 주장 중 하나는 AlphaFold 2(2021)가 진정한 변곡점이었지만, 그것이 무에서 나오지 않았다는 것이다(Gap 9 참조). 1세대 발효 화장품 시대 내내 AI for biology는 점진적으로 다른 분야에서 축적되고 있었다.
1990년대 QSAR(Quantitative Structure–Activity Relationship)·classical docking(AutoDock 등)이 약물 디자인의 표준 도구가 되었다. 2000년대 화학정보학(cheminformatics)과 머신러닝이 결합되며 ChEMBL·ZINC 같은 표준 화합물 라이브러리가 등장했다. 2010년대 후반 그래프 신경망(GNN)이 분자 구조 예측에 진입했고, 그 산출물의 정점이 [16]의 Cell 논문이다 — MIT의 Collins lab은 message passing neural network(MPNN)로 11만 분자를 스크리닝하여 새 항생제 halicin을 발견했다. 이 논문은 종종 "AI가 처음으로 새 항생제를 찾았다"는 헤드라인으로 소개되지만, 본질은 다르다 — 2020년 시점에 이미 AI는 합성 화학 라이브러리 안에서 새로운 활성 분자를 식별할 수 있었다.
이 흐름이 마이크로바이옴 화장품에 직접 적용되지 못한 이유는 데이터 부족이었다. 미생물 대사체(metabolite) 데이터베이스가 정비된 것은 [13]의 iHSMGC(integrated Human Skin Microbial Gene Catalog)가 한족 인구 코호트에서 10.9M 유전자를 카탈로그화한 시점부터다. 그리고 단백질-대사체 상호작용을 예측할 수 있는 도구가 등장한 것이 [9]의 AlphaFold 2이다. 두 가지가 같은 해에 등장한 것은 우연이 아니다 — 2021년이 이 책에서 반복적으로 등장할 "year zero"다(Chapter 5에서 본격적으로 풀어간다).
1.6 패러다임 전환 — 세 가지 축이 동시에 이동했다
1세대(발효)에서 2세대(데이터 중심)로의 전환을 마케팅 슬로건이 아니라 연구 패러다임의 축 이동으로 정직하게 그리면 다음 세 가지다.
축 1 — 단일 균주 → 생태계 군집. 1세대는 "이 균이 이 효능을 낸다"는 가설이었다. 2세대는 "이 부위의 이 균총 구성이 이 효능을 낸다"는 가설이다. [2]와 [5]이 이 전환의 첫 측정을 가능하게 했다.
축 2 — In vitro 추출물 → 생태계 신호 전달. 1세대는 발효 여과액의 추출물을 케라티노사이트 한 종에 적용하는 단순한 모델이었다. 2세대는 Cutibacterium acnes 균주가 분비한 펩타이드가 Staphylococcus epidermidis의 phenol-soluble modulin과 어떻게 상호작용하여 피부 면역계의 AHR·NF-κB 신호를 조정하는가 — multi-omics·multi-species 모델이다.
축 3 — 마케팅 주장 → 데이터 기반 가설. 1세대의 "100가지 효능" 언어는 검증 가능하지 않았다. 2세대의 가설은 "이 균주를 적용 시 4주 후 cheek 부위 Cutibacterium RT6 비율이 baseline 대비 X% 증가하며, 이는 transepidermal water loss(TEWL)와 r=Y의 상관을 갖는다"처럼 명시적이다. 이 명시성이 AI가 들어올 수 있는 표면을 만든다 — AI는 모호한 주장에는 손쓸 수 없고, 측정 가능한 endpoint에만 작동한다.
이 세 축은 독립적이지 않다. 시퀀싱 비용이 무너졌기 때문에 균총을 측정할 수 있었고, 균총을 측정할 수 있었기 때문에 생태계 신호 전달을 모델링할 수 있었고, 모델링이 가능해졌기 때문에 측정 가능한 가설이 의미를 가지게 되었다. 1세대와 2세대 사이의 경계는 단일 사건이 아니라 세 곡선이 동시에 임계점을 넘은 약 5년의 구간(2009–2014)이다.
1.7 그래서 1세대 발효 화장품은 구식인가 — 책 전체의 첫 번째 답
Brief A가 가장 강하게 던진 질문 — "기초 연구는 이제 다 구식이 된 건지" — 에 대한 이 책의 답은 아니오, 보완 관계다이다. 본격 논증은 Chapter 3와 Chapter 9에서 펼치지만, 이 챕터를 끝맺기 전에 핵심 골격은 짚고 가야 한다.
발효 화장품 1세대가 한 일 중 여전히 유효한 부분은 세 가지다. 첫째, 균주 분리·배양·동정의 wet-lab 자산은 AI의 ground truth다. AI는 예측하고 배양은 검증한다 — 검증 없는 예측은 시연(demo)에 그친다. 둘째, 항균·항염 표준 어세이는 endpoint 정의의 기반이다. AI 모델이 어떤 분자를 "anti-inflammatory candidate"라고 부를 때, 그 라벨은 결국 1980년대부터 표준화된 in vitro NF-κB·MMP·IL-6 어세이의 결과에서 나온다. 셋째, 임상 효능 평가의 endpoint 자체(filaggrin 발현, TEWL, 콜라겐 합성률, 홍반 지수) 또한 wet-lab 시대에 정의된 자산이다.
발효 화장품 1세대가 한 일 중 이제는 더 이상 유지되기 어려운 부분도 셋이다. 첫째, "단일 균주 발효물 vs 위약" 구도는 균주 해상도·부위 특이성·시간 동학을 잡아낼 수 없다. 둘째, "100가지 효능" 식 marketing-grade claim은 2024–2026 FTC·EU CTR 흐름에서 점점 더 방어 불가능해지고 있다. 셋째, 발효 여과액의 분자 기전을 알지 못한 채 30년을 보낸 산업 운영 패턴은 — AI가 그 분자 기전을 빠르게 채울 수 있는 시대에 — 더 이상 정당화되지 않는다.
이 책이 마지막 챕터(Chapter 12)에서 "신규 연구 기획 청사진"을 제시하는 이유는, 1세대의 가치 있는 자산(균주·어세이·endpoint)을 그대로 보존하면서 2세대의 데이터·AI·합성생물학을 어떻게 결합할 것인가 — 그 결합 양식이 곧 차세대 화장품 R&D의 차별화 축이기 때문이다.
1.8 한국 사례 — 메커니즘이 따라잡는 산업 사례
한국은 이 패러다임 전환의 특수한 사례를 갖는다 — 1세대 발효 화장품(설화수·후·SUM37)의 글로벌 시장 점유율을 만든 동시에, 2세대 데이터 중심 연구도 동시에 진행 중인 보기 드문 시장이다. [10]의 Communications Biology 논문은 COSMAX-Dankook-GIST 공동 작업으로 Lactobacillus rhamnosus IDCC 3201 균주에서 spermidine이 분비되며 이 spermidine이 사람 피부 진피의 콜라겐·엘라스틴 재구성을 유도한다는 메커니즘을 보였다. [11]의 EPI-7 임상 연구는 Epidermidibacterium keratini EPI-7 균주에서 유도한 포스트바이오틱이 12주 임상에서 주름·탄력 endpoint를 개선한다는 결과를 International Journal of Molecular Sciences에 게재했다.
이 두 논문은 한국 발효 화장품이 1세대의 "효능 있는 듯하다" 언어에서 2세대의 "이 균주의 이 분자가 이 endpoint를 이만큼 움직인다" 언어로 어떻게 이동하고 있는지를 보여주는 가장 명확한 사례다. Chapter 10이 한국 산업의 publication 비대칭(COSMAX가 publication-가시적인 반면 아모레퍼시픽·LG생활건강은 publication-비가시적)을 본격적으로 다룬다.
1.9 비전문가 독자를 위한 한 페이지 요약
이 챕터의 메시지를 한 페이지로 압축하면 다음과 같다.
1세대 발효 화장품(1980–2010년대 초)은 효모·유산균 발효 여과액의 경험적 효능을 상품화했지만, 그 효능의 분자 메커니즘은 30년간 거의 미지였다. 이 시기는 마케팅 언어가 과학 언어를 30년 앞서간 시대다.
2005–2014년 시퀀싱 비용이 약 1,000배 떨어지며 한 사람의 피부 생태계 전체를 읽는 일이 처음으로 가능해졌다. 2009–2012년 사이 [2], [5], [3], [8] 등 정초 논문이 잇따라 발표되며 피부 마이크로바이옴 연구는 "측정 도구를 갖춘 분야"가 되었다. 이 시기는 현미경을 갖춘 미생물학의 순간이라 부를 수 있다.
2021년 [9]의 AlphaFold 2를 비롯한 단백질 구조 예측 도구가 등장하며 미생물 대사체–피부 단백질 상호작용 예측이 처음으로 산업적 비용 구조에서 가능해졌다. 이 시기는 AI가 발효 화장품의 30년 메커니즘 공백을 압축할 수 있게 된 변곡점이다 — 그리고 책의 나머지 11개 챕터가 그 변곡점의 해부학이다.
발효는 끝나지 않았다. 마이크로바이옴 시대의 새로운 발효는 데이터가 균주를 고르고, AI가 분자를 예측하고, 합성생물학이 생산하고, 임상이 검증한다. 같은 단어, 완전히 다른 산업이다.
1.10 Open Questions — 이 책이 돌아올 세 가지 질문
이 챕터는 답하지 않고 후속 챕터로 넘기는 세 가지 질문을 명시적으로 남긴다.
Open Question 1 — 발효 여과액(fermentate) 성분은 이제 폐기되어야 하는가? Galactomyces·Bifida·Saccharomyces ferment filtrate는 여전히 유통되고 있고, 일부([17], [7])는 retrospective하게 분자 기전이 밝혀졌다. 그러나 비-Galactomyces 발효물 다수는 여전히 mechanism-deficit 상태다. 책의 답은 Chapter 5(AlphaFold 이후)와 Chapter 7(합성생물학)에서 — 발효물 자체보다는 그 안의 개별 활성 분자를 식별·정제·재합성하는 방향이 차세대 답이라는 것.
Open Question 2 — 균주 분리·배양·항균 테스트 같은 wet-lab 기초 연구는 구식인가? 책의 한 줄 답은 "아니오, AI의 ground truth로 더 중요해졌다." 본격 논증은 Chapter 3(NGS·메타지노믹스·culturomics)와 Chapter 9(임상 효능 검증)에서.
Open Question 3 — 1세대 발효 화장품의 마케팅 언어와 실제 임상 데이터 사이의 간극은 얼마나 컸는가? 그 간극은 2세대에서 좁혀지고 있는가? 책의 답은 Chapter 8(AI 제형 설계)과 Chapter 10(글로벌 기업 사례) 그리고 Chapter 12(연구 청사진)에서 — 정확히 측정 가능한 endpoint와 reproducibility 인프라가 없으면, 2세대도 1세대의 언어 비대칭을 그대로 반복할 위험이 있다.
이 세 질문은 책의 마지막 챕터까지 반복적으로 돌아온다. 1세대의 유산을 정직하게 평가하지 않으면 2세대의 가능성을 과대평가하기 쉽고, 2세대의 도구를 정직하게 평가하지 않으면 1세대의 자산을 부당하게 폐기하기 쉽다. 이 챕터는 그 양쪽 함정의 좌표를 미리 박아둔 것이다.
참고문헌
- Atallah, C., El Abiad, A., El Abiad, M., Nakad, M., & Assaf, J. C. (2025). Bioengineered Skin Microbiome: The Next Frontier in Personalized Cosmetics. Cosmetics, 12(5):205. doi:10.3390/cosmetics12050205.
- Costello, E. K., Lauber, C. L., Hamady, M., Fierer, N., Gordon, J. I., & Knight, R. (2009). Bacterial Community Variation in Human Body Habitats Across Space and Time. Science, 326(5960):1694–1697. doi:10.1126/science.1177486.
- Findley, K., Oh, J., Yang, J., Conlan, S., Deming, C., Meyer, J. A., Schoenfeld, D., Nomicos, E., Park, M., NISC Comparative Sequencing Program, Kong, H. H., & Segre, J. A. (2013). Topographic diversity of fungal and bacterial communities in human skin. Nature, 498(7454):367–370. doi:10.1038/nature12171.
- Fitz-Gibbon, S., Tomida, S., Chiu, B.-H., Nguyen, L., Du, C., Liu, M., Elashoff, D., Erfe, M. C., Loncaric, A., Kim, J., Modlin, R. L., Miller, J. F., Sodergren, E., Craft, N., Weinstock, G. M., & Li, H. (2013). Propionibacterium acnes strain populations in the human skin microbiome associated with acne35970-1/fulltext). Journal of Investigative Dermatology, 133(9):2152–2160. doi:10.1038/jid.2013.21.
- Grice, E. A., Kong, H. H., Conlan, S., Deming, C. B., Davis, J., Young, A. C., NISC Comparative Sequencing Program, Bouffard, G. G., Blakesley, R. W., Murray, P. R., Green, E. D., Turner, M. L., & Segre, J. A. (2009). Topographical and Temporal Diversity of the Human Skin Microbiome. Science, 324(5931):1190–1192. doi:10.1126/science.1171700.
- Grice, E. A., & Segre, J. A. (2011). The skin microbiome. Nature Reviews Microbiology, 9(4):244–253. doi:10.1038/nrmicro2537.
- Hashimoto-Hachiya, A., Furue, M., & Tsuji, G. (2022). Galactomyces Ferment Filtrate Potentiates an Anti-Inflammaging System in Keratinocytes. Journal of Clinical Medicine, 11(21):6338. doi:10.3390/jcm11216338.
- Human Microbiome Project Consortium (2012). Structure, function and diversity of the healthy human microbiome. Nature, 486(7402):207–214. doi:10.1038/nature11234.
- Jumper, J., Evans, R., Pritzel, A., Green, T., Figurnov, M., Ronneberger, O., Tunyasuvunakool, K., Bates, R., Žídek, A., Potapenko, A., et al. (2021). Highly accurate protein structure prediction with AlphaFold. Nature, 596(7873):583–589. doi:10.1038/s41586-021-03819-2.
- Kim, G., Kim, M., Kim, M., Park, C., Yoon, Y., Lim, D.-H., Yeo, H., Kang, S., Lee, Y.-G., Beak, N.-I., Lee, J., Kim, S., Kwon, J. Y., Choi, W. W., Lee, C., Yoon, K. W., Park, H., & Lee, D.-G. (2021). Spermidine-induced recovery of human dermal structure and barrier function by skin microbiome. Communications Biology, 4:231. doi:10.1038/s42003-020-01619-4.
- Kim, J., Lee, Y. I., Mun, S., Jeong, J., Lee, D.-G., Kim, M., Jo, H., Lee, S., Han, K., & Lee, J. H. (2023). Efficacy and Safety of Epidermidibacterium Keratini EPI-7 Derived Postbiotics in Skin Aging: A Prospective Clinical Study. International Journal of Molecular Sciences, 24(5):4634. doi:10.3390/ijms24054634.
- Kobyliak, N., Conte, C., Cammarota, G., Haley, A. P., Styriak, I., Gaspar, L., Fusek, J., Rodrigo, L., & Kruzliak, P. (2016). Probiotics in prevention and treatment of obesity: a critical view. Nutrition & Metabolism, 13:14. doi:10.1186/s12986-016-0067-0.
- Li, Z., Xia, J., Jiang, L., Tan, Y., An, Y., Zhu, X., Ruan, J., Chen, Z., Zhen, H., Ma, Y., Jie, Z., Xiao, L., Yang, H., Wang, J., Kristiansen, K., Xu, X., Jin, L., Nie, C., Krutmann, J., Liu, X., & Wang, J. (2021). Characterization of the human skin resistome and identification of two microbiota cutotypes. Microbiome, 9:47. doi:10.1186/s40168-020-00995-7.
- Oh, J., Byrd, A. L., Deming, C., Conlan, S., NISC Comparative Sequencing Program, Kong, H. H., & Segre, J. A. (2014). Biogeography and individuality shape function in the human skin metagenome. Nature, 514(7520):59–64. doi:10.1038/nature13786.
- Oh, J., Byrd, A. L., Park, M., NISC Comparative Sequencing Program, Kong, H. H., & Segre, J. A. (2016). Temporal Stability of the Human Skin Microbiome30399-3). Cell, 165(4):854–866. doi:10.1016/j.cell.2016.04.008.
- Stokes, J. M., Yang, K., Swanson, K., Jin, W., Cubillos-Ruiz, A., Donghia, N. M., MacNair, C. R., French, S., Carfrae, L. A., Bloom-Ackermann, Z., Tran, V. M., Chiappino-Pepe, A., Badran, A. H., Andrews, I. W., Chory, E. J., Church, G. M., Brown, E. D., Jaakkola, T. S., Barzilay, R., & Collins, J. J. (2020). A Deep Learning Approach to Antibiotic Discovery30102-1). Cell, 180(4):688–702.e13. doi:10.1016/j.cell.2020.01.021.
- Takei, K., Mitoma, C., Hashimoto-Hachiya, A., Tsuji, G., Takahara, M., & Furue, M. (2015). Galactomyces fermentation filtrate prevents T helper 2-mediated reduction of filaggrin in an aryl hydrocarbon receptor-dependent manner. Clinical and Experimental Dermatology, 40(7):786–793. doi:10.1111/ced.12635.