Chapter 2: 피부 마이크로바이옴 — 부위·균종·항상성의 지도
2.1 왜 "피부 마이크로바이옴"이라는 개념이 필요한가
피부는 평균 1.8m²의 표면적과 수많은 주름·모공·땀샘으로 이뤄진 복잡한 환경이다. 이 표면에는 사람 세포 수에 견줄 만한 미생물이 살고 있고, 그들은 단순한 "오염"이 아니라 피부 면역과 장벽 기능을 조율하는 공생 생태계다. 1세대 발효 화장품(Chapter 1)이 "어떤 균주의 어떤 발효물이 효능을 가지는가"를 물었다면, 2세대 마이크로바이옴 화장품은 질문 자체를 바꿨다. "어떤 미생물 군집이 어떤 상태의 피부를 만드는가, 그리고 그 군집을 어떻게 조절할 것인가."
이 전환은 1990년대 후반까지 거슬러 올라가지만, 결정적인 변곡점은 2009년이었다. 그해 두 편의 Science 논문이 같은 메시지를 다른 각도에서 던졌다 — 피부에는 부위마다 다른 군집이 산다는 사실, 그리고 그 군집은 개인보다 부위에 더 강하게 의존한다는 사실이다 [7] [4]. 이 두 발견은 그 이후 모든 피부 마이크로바이옴 화장품 R&D의 출발 좌표가 됐다.
이 챕터의 정량적 핵심 3가지 1. 부위가 개체보다 강하다: 손바닥의 군집은 다른 사람 손바닥과 더 닮았지, 같은 사람의 이마와 닮지 않았다 [4]. 2. 사람 사이 변이는 크지만 시간적 안정성은 높다: 한 사람의 피지 부위 균주는 1–2년 동안 80% 이상 동일하게 유지된다 [18]. 3. 종(species)으로는 부족하다 — strain 단위가 표현형을 결정한다: 여드름 환자와 건강인의 Cutibacterium acnes 총량은 비슷하지만, 그 안의 strain 분포가 다르다 [6].
이 챕터의 목적은 책의 나머지가 반복적으로 참조할 "지도" 를 그리는 것이다. 부위별 생태(2.2) → 핵심 균종(2.3) → 개체 간 변이와 인종 차이(2.4) → "Dysbiosis"라는 모호한 단어의 해부(2.5) → 질환과의 인과/상관(2.6) → 그리고 아직 답이 없는 질문들(2.7). AI 모델(Chapter 4–6)이 무엇을 학습하고 어디서 실패하는지 이해하려면 먼저 이 지도가 필요하다.
2.2 부위 프레임워크 — sebaceous, moist, dry
피부 마이크로바이옴의 가장 단단한 경험 법칙은 부위가 모든 것을 지배한다는 것이다. [7]는 건강한 성인 10명의 20개 부위에서 16S rRNA를 시퀀싱하여, 피부를 물리·생리학적 특성에 따라 세 부류로 분류했다.
Sebaceous (피지선이 많은 부위) — 이마, 미간, 코, 등 윗부분. 피지(sebum)가 풍부한 환경은 지질을 분해할 수 있는 Cutibacterium acnes (구 Propionibacterium acnes)가 점유한다. 피지선 단위(pilosebaceous unit) 안에서 C. acnes가 70% 이상의 상대 풍부도를 점하는 경우가 흔하다 [2].
Moist (땀이 많고 습한 부위) — 겨드랑이, 팔꿈치 안쪽, 무릎 뒤, 발가락 사이. Staphylococcus와 Corynebacterium이 우점한다. 습도와 염도가 높은 환경이 이들 그람양성균에 유리하다.
Dry (건조한 부위) — 팔뚝, 손바닥, 다리. 가장 다양한 군집을 가진다. 평균 44종 정도가 공존하며 (반대로 retroauricular crease — 귀 뒤 주름 — 는 평균 19종으로 가장 적다 [7]), Proteobacteria와 Flavobacteriales가 다른 부위보다 두드러진다.
흥미롭게도 [4]가 같은 해 Science에 발표한 결과는 이 부위 프레임워크가 신체 부위 전체에 일반화됨을 보였다 — 피부·구강·장·생식기를 통틀어, 군집을 가장 강하게 결정하는 변수는 부위 > 개인 > 시간 순이었다. 즉 당신의 이마 미생물은 옆 사람의 이마와 더 닮았지, 당신의 팔뚝과 닮지 않았다.
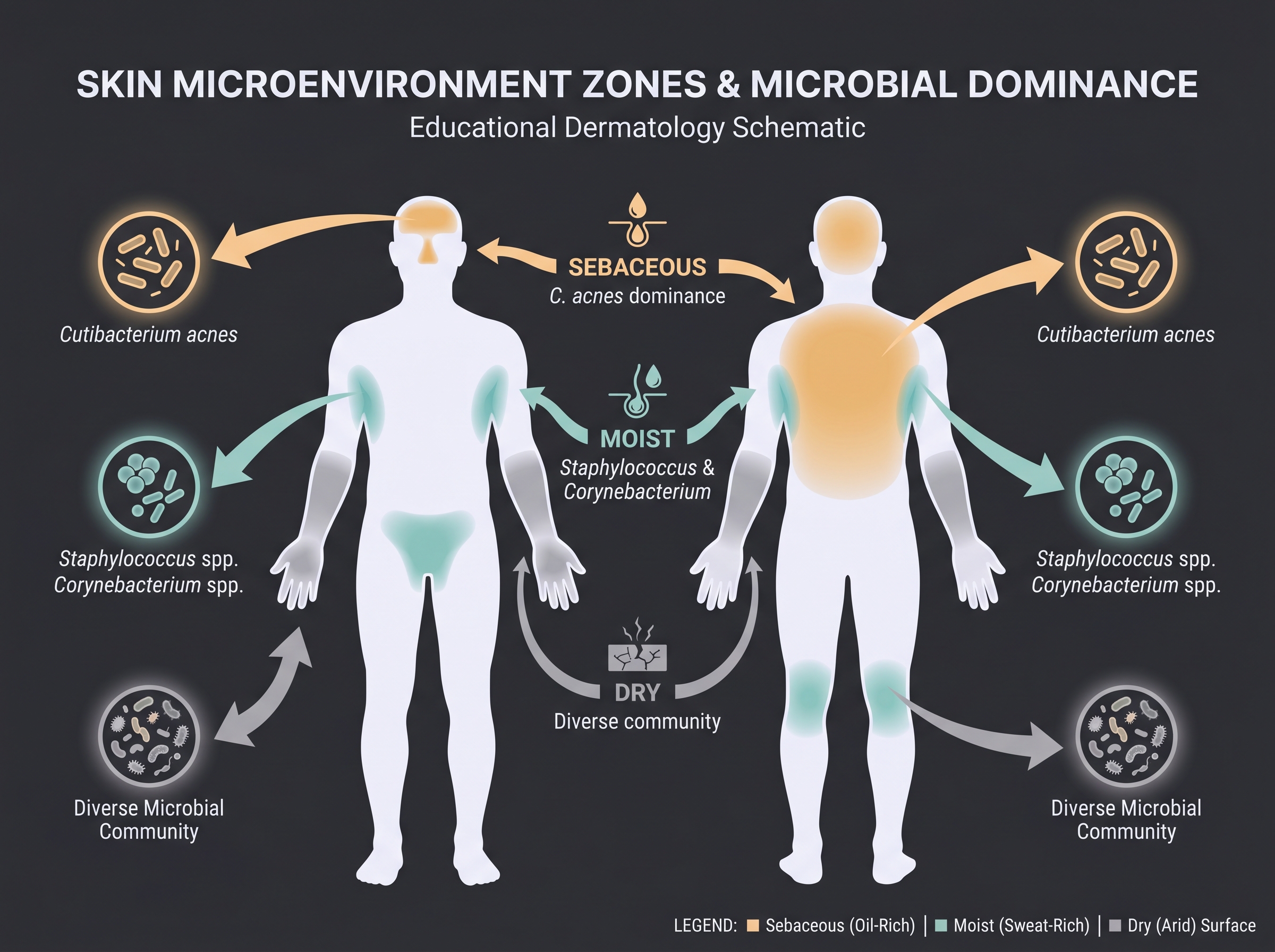
이 프레임워크는 단순하지만 강력하다. 화장품 R&D 관점에서, "이 제품은 어느 부위에 쓰는가"가 곧 "어떤 미생물 군집과 상호작용하는가"를 80% 결정한다. 페이셜 세럼이 만나는 미생물 군집과 데오도란트가 만나는 미생물 군집은 거의 완전히 다르다. 클렌징 제품의 균형(microbiome-friendly cleansing)을 평가할 때조차, T-zone과 U-zone을 같은 endpoint로 묶으면 신호가 희석된다.
하지만 [7]가 만든 이 세 부류 분류는 연속 변수의 이산화라는 한계를 가진다. 실제로 피지 분비량은 부위 간에 연속적으로 변하고, 개인의 피지 수준은 유전·호르몬·계절에 따라 달라진다. 후속 AI 모델(Chapter 6)이 자주 부딪히는 어려움 중 하나는, sebaceous/moist/dry라는 라벨을 학습할지 sebum, transepidermal water loss(TEWL), pH 같은 연속 측정값을 학습할지의 트레이드오프다. 양쪽 다 가능하지만, 후자가 더 본질에 가까운 표현이다.
2.3 핵심 균종 — Cutibacterium acnes, Staphylococcus epidermidis, Malassezia
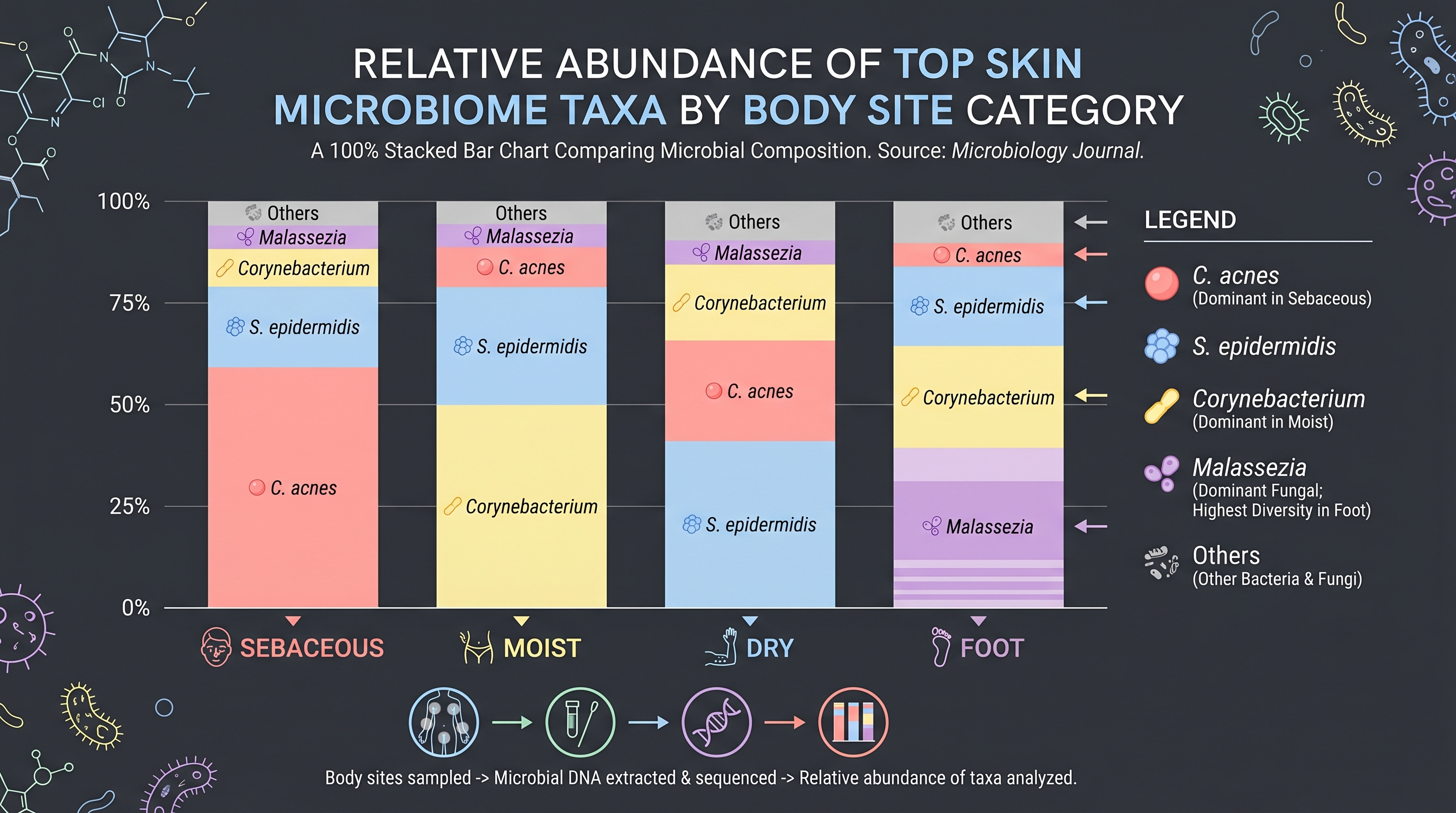
피부 마이크로바이옴에는 수백 종이 살지만, 화장품 R&D의 거의 모든 논의가 결국 세 가지 균(또는 균속)으로 수렴한다. 이들은 단순히 풍부한 것이 아니라 기능적으로 결정적이기 때문이다.
2.3.1 Cutibacterium acnes — 피지선의 양면
2016년 Propionibacterium acnes에서 Cutibacterium acnes로 재명명된 이 균은 [2], 피지선 부위에서 가장 흔하고 또한 가장 오해받는 균이다. 30년 동안 화장품·피부과 산업은 "여드름 = P. acnes"라는 단순 등식 위에 항균 전략을 쌓아왔다. 그러나 그 전제는 strain 수준에서 검증되지 않은 채였다.
[6]이 49명의 여드름 환자와 52명의 건강 대조군의 모낭피지선 단위(pilosebaceous unit)를 strain 수준에서 분석했을 때, 충격적인 결과가 나왔다 — 두 그룹의 C. acnes 총량은 통계적으로 다르지 않았다. 차이는 strain 분포에 있었다. RT4·RT5 ribotype은 여드름 환자에서 풍부했고, RT6는 건강한 피부에서 풍부했다. 즉 C. acnes는 적이 아니라 이중적 존재다 — 어떤 strain은 보호적, 어떤 strain은 병원성이다.
이 발견은 화장품 R&D 전략을 근본적으로 뒤집었다. "C. acnes를 죽이는" 항균 접근은 보호 strain까지 함께 제거해 장기적으로 피부 생태계를 더 불안정하게 만들 수 있다. 대신 새로운 전략 — strain-selective phage cocktail, RoxP(C. acnes가 분비하는 천연 항산화제)를 과발현하는 엔지니어드 strain, ribotype별 진단·맞춤 처방 — 들이 등장했다. (이 산업 분기는 Chapter 10에서 자세히 다룬다.)
2.3.2 Staphylococcus epidermidis — 보호적 공생자
S. epidermidis는 호기성 피부 거주균의 90%까지 차지할 수 있는, 가장 흔한 피부 commensal이다 [2]. 1990년대까지 이 균은 임상 미생물학에서 "병원 감염의 contaminant" 정도로 취급됐다. 그러나 2009년 [13]가 mechanism 수준에서 그 평가를 뒤집었다.
[13]가 보여준 회로는 다음과 같다. S. epidermidis의 세포벽 구성성분인 lipoteichoic acid(LTA)는 keratinocyte의 Toll-like receptor 2(TLR2)에 결합한다. TLR2 신호는 같은 세포 내에서 TLR3 신호를 억제한다. TLR3는 손상된 피부에서 self-RNA에 반응해 과도한 염증을 일으키는 경로다. 즉 S. epidermidis가 표면에 살고 있으면, 피부가 손상됐을 때 염증 반응이 자동으로 완화된다. 이는 화장품·피부과학이 30년간 광고해 온 "프로바이오틱이 피부에 좋다"는 주장에 처음으로 분자 수준의 메커니즘을 제공했다.
이후 [15]는 germ-free 마우스 실험으로 S. epidermidis가 피부 T-cell의 IL-1 의존적 면역 교육에 필수적임을 보였고, [16]의 Gallo 그룹은 S. hominis A9 같은 응고효소 음성 Staphylococcus(CoNS) 균주가 항균 펩타이드를 분비해 S. aureus의 정착을 막는다는 사실을 입증했다. S. epidermidis와 그 친척들은 단순히 "공존하는 무해한 균"이 아니다 — 그들은 국지 면역계의 일부다.
하지만 여기에도 미묘한 함정이 있다. S. epidermidis의 일부 strain은 카테터·인공관절 같은 의료기기에서 biofilm을 형성하여 병원감염을 일으킨다. S. aureus와 마찬가지로 S. epidermidis도 strain에 따라 표현형이 크게 갈린다. 화장품에서 S. epidermidis 후생물(postbiotic) 또는 동등물(equivalent) 성분을 사용할 때, 어떤 strain의 무엇을 분리·정제했는가는 마케팅 카피보다 훨씬 더 중요하다.
2.3.3 Malassezia — 진균의 거장
박테리아 일변도의 초기 마이크로바이옴 연구를 [5]가 흔들어 놓았다. 진균 ITS1과 박테리아 16S를 동시에 시퀀싱한 이 연구는, 피부 진균 군집의 90% 이상이 Malassezia 한 속에 속한다는 사실을 밝혔다. 손·팔·몸통의 11개 부위에서 Malassezia가 진균 리드의 80% 이상을 차지했고, 반면 발 부위는 Aspergillus, Cryptococcus, Rhodotorula가 섞이며 2–5배 더 다양했다.
Malassezia는 지질에 의존하는 진균이다. 자체적으로 지방산을 합성하지 못해 피부 피지의 중성지방을 분해해 살아간다. 이 과정에서 분비되는 lipase가 자유 지방산을 만들고, 그중 일부(특히 oleic acid)는 일부 사람의 피부에서 자극과 비듬·지루성 피부염을 유발한다 [19]. 비듬 샴푸의 핵심 활성 성분(zinc pyrithione, ketoconazole, selenium sulfide)이 모두 항진균제인 이유다.
그러나 Malassezia는 동시에 정상 피부의 거주균이기도 하다. C. acnes와 마찬가지로 "있냐 없냐"가 아니라 "어떤 종·어떤 양"이 문제다. M. restricta와 M. globosa는 가장 흔한 두 종이지만, 둘 사이의 비율과 활성도가 지루성 피부염·아토피·말라쎄지아 모낭염의 임상 표현형을 결정한다. 박테리아·진균을 한 생태계로 다루는 멀티킹덤 모델링은 Chapter 6의 핵심 주제 중 하나다.
2.4 개체 간 변이 — 쌍둥이, 인종, 그리고 동아시아의 "숨겨진 유전자"
부위가 군집의 80%를 결정한다면, 나머지 20%는 무엇이 결정하는가? 답은 복잡하다. 유전·연령·호르몬·지역·생활습관·화장품 사용 — 모두 기여한다. 그러나 가장 흥미로운 단일 사실은 [14]의 연구에서 나왔다.
[14]은 822명의 중국 한족 피부에서 shotgun 메타지노믹스 데이터를 수집해, 기존 538명의 북미 데이터와 합쳐 integrated Human Skin Microbial Gene Catalog (iHSMGC) 를 만들었다. 총 1,093만 개의 미생물 유전자가 목록화됐고, 그중 약 488만 개 — 즉 44.6% — 가 기존 카탈로그에 없던 새 유전자였다. 더 놀라운 것은 Moraxella osloensis가 중국인 코호트에서 두 번째로 풍부한 균이었지만 북미 데이터에는 거의 부재한다는 사실이었다. 저자들은 두 가지 "cutotype"을 정의했다 — Moraxella osloensis 유형과 C. acnes 유형 — 그리고 호스트 의존적 영양 사슬 가설로 이 분기를 설명했다.
이 발견의 의미는 깊다. 북미·유럽 코호트만으로 학습된 모든 ML 모델은 동아시아 소비자의 약 45%에 해당하는 미생물 유전자를 본 적이 없다. 한국·중국·일본 기업이 자체 메타지노믹스 코호트를 구축하는 전략적 동기가 여기에 있다. (이 비대칭이 한국 산업·학계에서 어떻게 작동하는지는 Chapter 10에서 다룬다.)
쌍둥이 연구는 또 다른 각도를 제공한다. 일란성 쌍둥이의 피부 마이크로바이옴은 이란성 쌍둥이보다 더 비슷하지만, 차이는 부위와 연령 효과에 비하면 작다. 즉 유전은 약하지만 측정 가능한 효과를 가진다. 가족·룸메이트 효과(공유된 가정 환경)도 통계적으로 유의하다. 이는 마이크로바이옴이 개인의 정체성이라기보다 개인 × 환경의 함수임을 시사한다.
마지막으로 시간적 안정성. [18]은 HMP 코호트의 12명을 1–2년 후 다시 샘플링하여, strain 수준에서 80% 이상이 동일하게 유지됨을 보였다. 피지 부위가 가장 안정적이고 발이 가장 불안정했다. 이는 두 가지 함의를 가진다 — 첫째, 마이크로바이옴은 "당신의 것"이라 부를 만큼 충분히 안정적이고, 둘째, 화장품으로 이 안정성을 흔들기는 어렵다. "마이크로바이옴을 회복시킨다"는 마케팅 카피는 자주 이 안정성과 충돌한다.
2.5 "Dysbiosis"라는 단어를 해부하기
마이크로바이옴 화장품 마케팅의 핵심 단어가 "dysbiosis(균총 이상)"다. 광고는 dysbiosis가 여드름·아토피·노화의 원인이고, 제품이 이를 "균형"으로 되돌린다고 주장한다. 그러나 학술 문헌에서 dysbiosis는 놀랍도록 모호한 단어다.
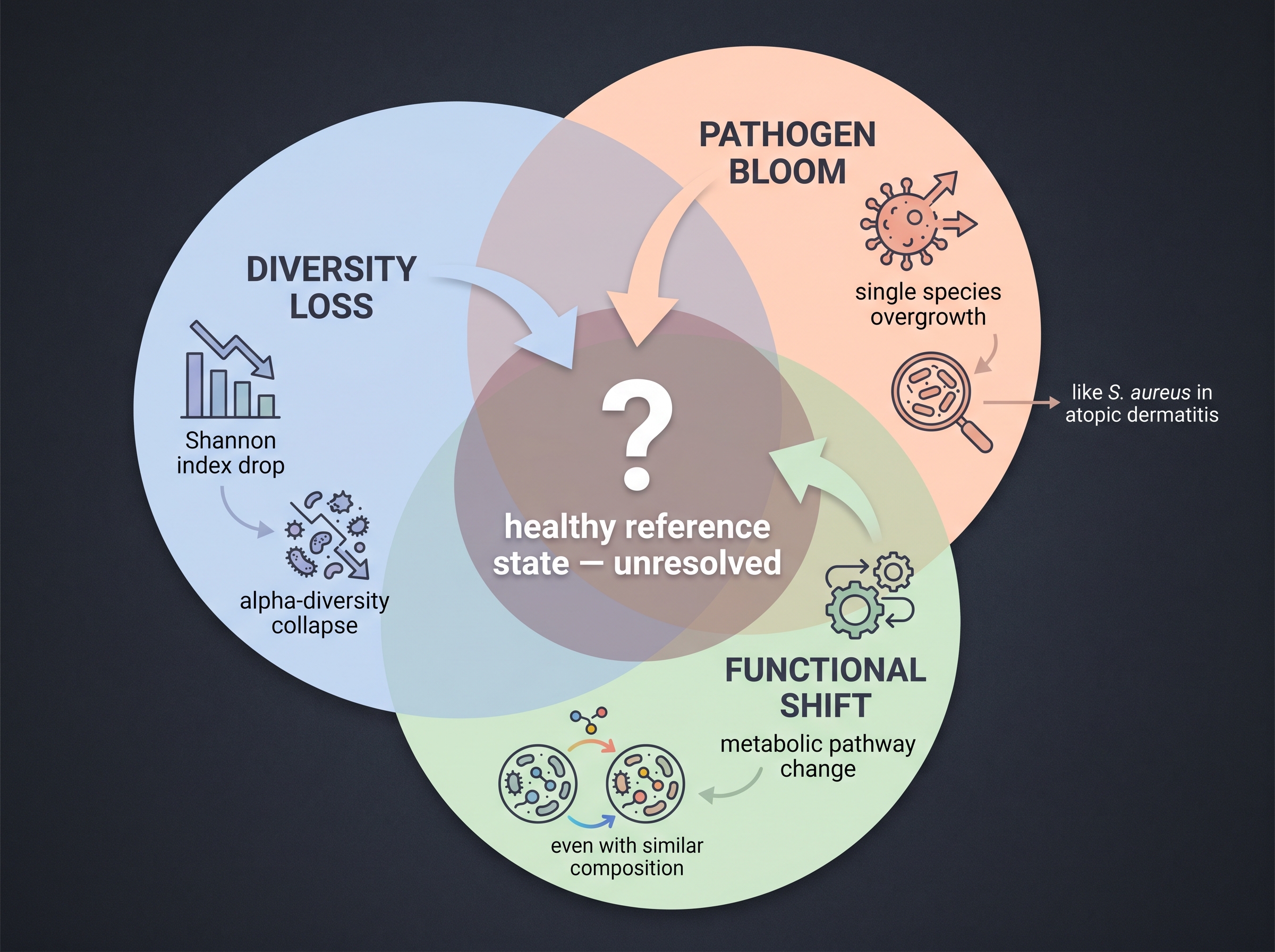
조작적 정의는 적어도 세 가지다 [2]:
- 다양성 감소 — Shannon diversity가 건강 대조군 평균보다 낮음.
- 병원성 균의 과증식 — S. aureus가 S. epidermidis를 대체하는 등.
- 기능적 dysbiosis — 풍부도와 상관없이 유전자/대사 기능 프로파일이 비정상.
문제는 이 세 정의가 같은 데이터에서 다른 결론을 낼 수 있다는 점이다. 예를 들어 [11]의 아토피피부염 코호트는 flare 시점에 S. aureus가 폭증하지만 동시에 Shannon diversity는 감소한다. 치료 후 diversity는 회복되지만 S. aureus가 완전히 사라지기 전부터 임상 증상은 호전된다. 즉 "dysbiosis가 호전됐다"는 명제는, 어느 정의를 쓰는지에 따라 다른 시점을 가리킨다.
더 어려운 문제는 참조 상태(reference state)다. "건강한" 피부 마이크로바이옴이 무엇인지에 대한 합의된 기준이 없다. HMP는 북미 건강 성인을 정의했고, iHSMGC는 한족을 추가했지만, 연령·계절·생활환경·이전 화장품 사용 이력을 모두 통제한 표준 코호트는 존재하지 않는다. 어떤 화장품 임상연구가 "dysbiosis 개선"을 endpoint로 잡으려면, 그 자체로 어떤 정량적 기준을 만족해야 dysbiosis인지, 또 어떤 기준을 만족해야 회복인지를 미리 정의해야 한다. 현재 발표된 화장품 임상에서 이런 사전 정의가 명시된 사례는 드물다 [1].
[3]는 이 모호성을 더 강하게 표현했다 — "dysbiosis는 미생물 군집의 어떤 통계적 일탈이든 가리킬 수 있는 용어이며, 따라서 그 자체로는 인과적 주장을 뒷받침할 수 없다." 이 책은 dysbiosis라는 단어를 사용할 때마다 어느 정의를 사용하는지 명시하려 노력하며, 모호한 마케팅 용법과 조작적 정의를 분리해 다룬다.
2.6 질환과의 연결 — 상관과 인과의 경계
dysbiosis가 모호하더라도, 마이크로바이옴과 피부 질환의 연관성은 잘 확립돼 있다. 다만 그 연관성을 어떻게 해석하는지가 중요하다.
여드름. C. acnes strain 분포 변화가 가장 강한 연관 신호다 [6]. RT4·RT5 ribotype은 여드름 병변에 풍부하고, 이들은 hyaluronate lyase·CAMP factor 같은 가능한 병원성 인자를 가진다. 그러나 strain 변화가 여드름을 일으키는가, 여드름의 결과로 strain 분포가 바뀌는가는 아직 결정되지 않았다. 인과 방향은 모낭피지선 단위의 미세환경(피지 조성, 산소 농도)과 strain 적합도 간의 상호작용이며, 단일 방향 화살표로 정리되지 않는다.
아토피피부염(AD). [11]가 처음 정량화한 모델은 명확하다 — flare 시점에 S. aureus가 폭증하고, S. epidermidis 같은 보호 commensal이 감소한다. 그러나 이 변화가 AD의 원인인지 결과인지는 여전히 활발한 논쟁 주제다. Filaggrin 유전자 변이 같은 호스트 요인이 표피 장벽을 약하게 만들면, S. aureus가 정착하기 쉬워진다 — 이 관점에서 마이크로바이옴 변화는 호스트 결함의 표지자(marker)이지 원동력(driver)이 아니다. 반면 [16]의 보호 Staphylococcus 접근은 마이크로바이옴 자체를 직접 조작해서 임상 개선을 보였고 — 이는 마이크로바이옴이 수정 가능한 인과 요인의 일부임을 시사한다.
이 두 관점은 배타적이지 않다. 가장 그럴듯한 모델은 host × microbiome × environment의 다인성(multifactorial) 회로다. AD는 이 회로가 자기증폭 루프(filaggrin 결손 → 장벽 손상 → S. aureus 증식 → 더 큰 장벽 손상)에 갇힌 상태다. 마이크로바이옴 화장품은 이 루프의 한 노드를 건드릴 수 있지만, 다른 노드(예: 호스트 유전형)는 건드릴 수 없다.
주사(Rosacea). Demodex 진드기와 그 진드기가 옮기는 Bacillus oleronius에 대한 혈청 반응성이 주사 환자에서 82.6%, 대조군에서 26.9%다 [12]. 이는 강한 연관 신호지만, 인과 방향은 — 다시 — 명확하지 않다. 주사 환자의 피부 환경이 Demodex 증식을 허용하는 것인지, Demodex가 주사를 일으키는 것인지의 구분은 아직 결정되지 않았다.
지루성 피부염. Malassezia, 특히 M. restricta의 풍부도 증가와 강하게 연관된다 [19]. 이 경우는 인과의 증거가 비교적 강하다 — 항진균 치료가 임상 증상을 호전시킨다.
이 질환들의 공통점은 마이크로바이옴 변화가 일관되게 관찰되지만, 그것이 원인인지 결과인지는 질환마다 다르고, 종종 양방향이라는 점이다. 화장품 R&D 관점에서 이 구분은 결정적이다 — 결과를 바꾸는 화장품은 단기적 증상 완화를, 원인을 바꾸는 화장품은 (가능하다면) 근본적 개선을 약속한다. 그러나 대부분의 시판 마이크로바이옴 화장품은 어느 쪽도 명시하지 않은 채 "균형을 회복한다"고만 주장한다.
2.7 Open Questions — 이 챕터가 끝나도 답이 없는 것들
지도 그리기는 끝났지만, 여전히 빈 칸이 많다. 이 책의 나머지 챕터들은 다음 세 질문을 반복적으로 다시 만난다.
Q1. Dysbiosis를 어떻게 조작화할 것인가? Shannon diversity, 특정 균의 ratio, 기능적 프로파일 거리 — 어떤 단일 지표가 임상 endpoint와 가장 잘 상관하는가? 그리고 그 지표를 충분히 안정적으로 측정할 수 있는가? Chapter 3(NGS의 방법론적 한계)와 Chapter 9(임상 endpoint 설계)가 이 질문을 다시 다룬다.
Q2. 개체 간 변이를 어떻게 해석할 것인가 — 노이즈인가 신호인가? "이 사람의 마이크로바이옴은 이 사람의 것"이라는 정체성 관점은 personalized cosmetic의 마케팅 기반이다. 그러나 그 변이의 얼마나 많은 부분이 측정 잡음·환경 변동·검출 한계로 설명 가능한가? Chapter 6(상호작용 모델링)과 Chapter 9(임상 효능 검증)가 이 질문에 답을 시도한다.
Q3. 시간적 안정성과 화장품의 효력은 어떻게 양립하는가? [18]은 마이크로바이옴이 1–2년 동안 80% 이상 안정적임을 보였다. 만약 화장품이 마이크로바이옴을 "회복"시킨다면, 그 회복은 영구적인가 일시적인가? 사용을 중단하면 원래 상태로 돌아가는가? 이 질문은 마이크로바이옴 화장품의 장기적 가치 제안의 핵심이다. Chapter 9와 Chapter 12가 이 질문을 직접 다룬다.
이 세 질문은 책의 나머지 파트에서 점점 더 구체적인 모습으로 다시 나타난다. AI(Part II)는 이 질문들에 새로운 답을 시도하지만 동시에 새로운 형태의 같은 한계에 부딪힌다. 합성생물학과 임상 검증(Part III)은 답을 강제하는 실험적 압력을 가한다. 산업(Part IV)은 답이 없는 채로 의사결정을 내려야 하는 현실을 보여준다.
지도는 시작이지 끝이 아니다. 다음 챕터(Chapter 3)에서 우리는 이 지도를 그린 방법 — NGS, 메타지노믹스, 그리고 부활하는 culturomics — 를 다시 들여다본다.
참고문헌
- Atallah, C., Charcosset, C., Greige-Gerges, H. (2025). Bioengineered Skin Microbiome — A Critical Review on Skin Microbiome Modulation Strategies. Cosmetics, 12(5), 205. DOI: 10.3390/cosmetics12050205.
- Byrd, A. L., Belkaid, Y., Segre, J. A. (2018). The human skin microbiome. Nature Reviews Microbiology, 16(3), 143–155. DOI: 10.1038/nrmicro.2017.157.
- Carmona-Cruz, S., Orozco-Covarrubias, L., Saez-de-Ocariz, M. (2022). The Human Skin Microbiome in Selected Cutaneous Diseases. Frontiers in Cellular and Infection Microbiology, 12, 834135. DOI: 10.3389/fcimb.2022.834135. [Carmona-Cruz et al., 2022]
- Costello, E. K., Lauber, C. L., Hamady, M., Fierer, N., Gordon, J. I., Knight, R. (2009). Bacterial Community Variation in Human Body Habitats Across Space and Time. Science, 326(5960), 1694–1697. DOI: 10.1126/science.1177486.
- Findley, K., Oh, J., Yang, J., Conlan, S., Deming, C., Meyer, J. A., et al. (2013). Topographic diversity of fungal and bacterial communities in human skin. Nature, 498(7454), 367–370. DOI: 10.1038/nature12171.
- Fitz-Gibbon, S., Tomida, S., Chiu, B.-H., Nguyen, L., Du, C., Liu, M., et al. (2013). Propionibacterium acnes strain populations in the human skin microbiome associated with acne35970-1/fulltext). Journal of Investigative Dermatology, 133(9), 2152–2160. DOI: 10.1038/jid.2013.21.
- Grice, E. A., Kong, H. H., Conlan, S., Deming, C. B., Davis, J., Young, A. C., et al. (2009). Topographical and Temporal Diversity of the Human Skin Microbiome. Science, 324(5931), 1190–1192. DOI: 10.1126/science.1171700.
- Grice, E. A., Segre, J. A. (2011). The skin microbiome. Nature Reviews Microbiology, 9(4), 244–253. DOI: 10.1038/nrmicro2537. [Grice & Segre, 2011]
- Haykal, D., Flament, F., Amar, D., Cartier, H., Kourosh, A. S., Lee, S., Rowland-Payne, C. (2025). Cosmetogenomics unveiled: a systematic review of AI, genomics, and the future of personalized skincare. Frontiers in Artificial Intelligence, 8, 1660356. DOI: 10.3389/frai.2025.1660356.
- Human Microbiome Project Consortium (2012). Structure, function and diversity of the healthy human microbiome. Nature, 486(7402), 207–214. DOI: 10.1038/nature11234. [HMP Consortium, 2012]
- Kong, H. H., Oh, J., Deming, C., Conlan, S., Grice, E. A., Beatson, M. A., et al. (2012). Temporal shifts in the skin microbiome associated with disease flares and treatment in children with atopic dermatitis. Genome Research, 22(5), 850–859. DOI: 10.1101/gr.131029.111.
- Lacey, S., Kavanagh, S., Powell, S. C. (2014). Correlation between serum reactivity to Demodex-associated Bacillus oleronius proteins, and altered sebum levels and Demodex populations in erythematotelangiectatic rosacea patients. Journal of Medical Microbiology, 63(11), 1456–1462. DOI: 10.1099/jmm.0.073262-0.
- Lai, Y., Di Nardo, A., Nakatsuji, T., Leichtle, A., Yang, Y., Cogen, A. L., et al. (2009). Commensal bacteria regulate Toll-like receptor 3-dependent inflammation after skin injury. Nature Medicine, 15(12), 1377–1382. DOI: 10.1038/nm.2062.
- Li, Z., Xia, J., Jiang, L., Tan, Y., An, Y., Zhu, X., et al. (2021). Characterization of the human skin resistome and identification of two microbiota cutotypes. Microbiome, 9(1), 47. DOI: 10.1186/s40168-020-00995-7. [Li et al., 2021]
- Naik, S., Bouladoux, N., Wilhelm, C., Molloy, M. J., Salcedo, R., Kastenmuller, W., et al. (2012). Compartmentalized Control of Skin Immunity by Resident Commensals. Science, 337(6098), 1115–1119. DOI: 10.1126/science.1225152.
- Nakatsuji, T., Chen, T. H., Narala, S., Chun, K. A., Two, A. M., Yun, T., et al. (2017). Antimicrobials from human skin commensal bacteria protect against Staphylococcus aureus and are deficient in atopic dermatitis. Science Translational Medicine, 9(378), eaah4680. DOI: 10.1126/scitranslmed.aah4680.
- Oh, J., Byrd, A. L., Deming, C., Conlan, S., NISC Comparative Sequencing Program, Kong, H. H., Segre, J. A. (2014). Biogeography and individuality shape function in the human skin metagenome. Nature, 514(7520), 59–64. DOI: 10.1038/nature13786. [Oh et al., 2014]
- Oh, J., Byrd, A. L., Park, M., NISC Comparative Sequencing Program, Kong, H. H., Segre, J. A. (2016). Temporal Stability of the Human Skin Microbiome30399-3). Cell, 165(4), 854–866. DOI: 10.1016/j.cell.2016.04.008.
- Smith, A. (2025). Skin Microbiome in Health and Disease — A Comprehensive Review. Microorganisms, 13(1), Jan 2025. [Smith, 2025]