Chapter 9: In Silico에서 임상까지 — ex vivo, 임상 시뮬레이션, 효능 검증
이 챕터를 왜 읽는가
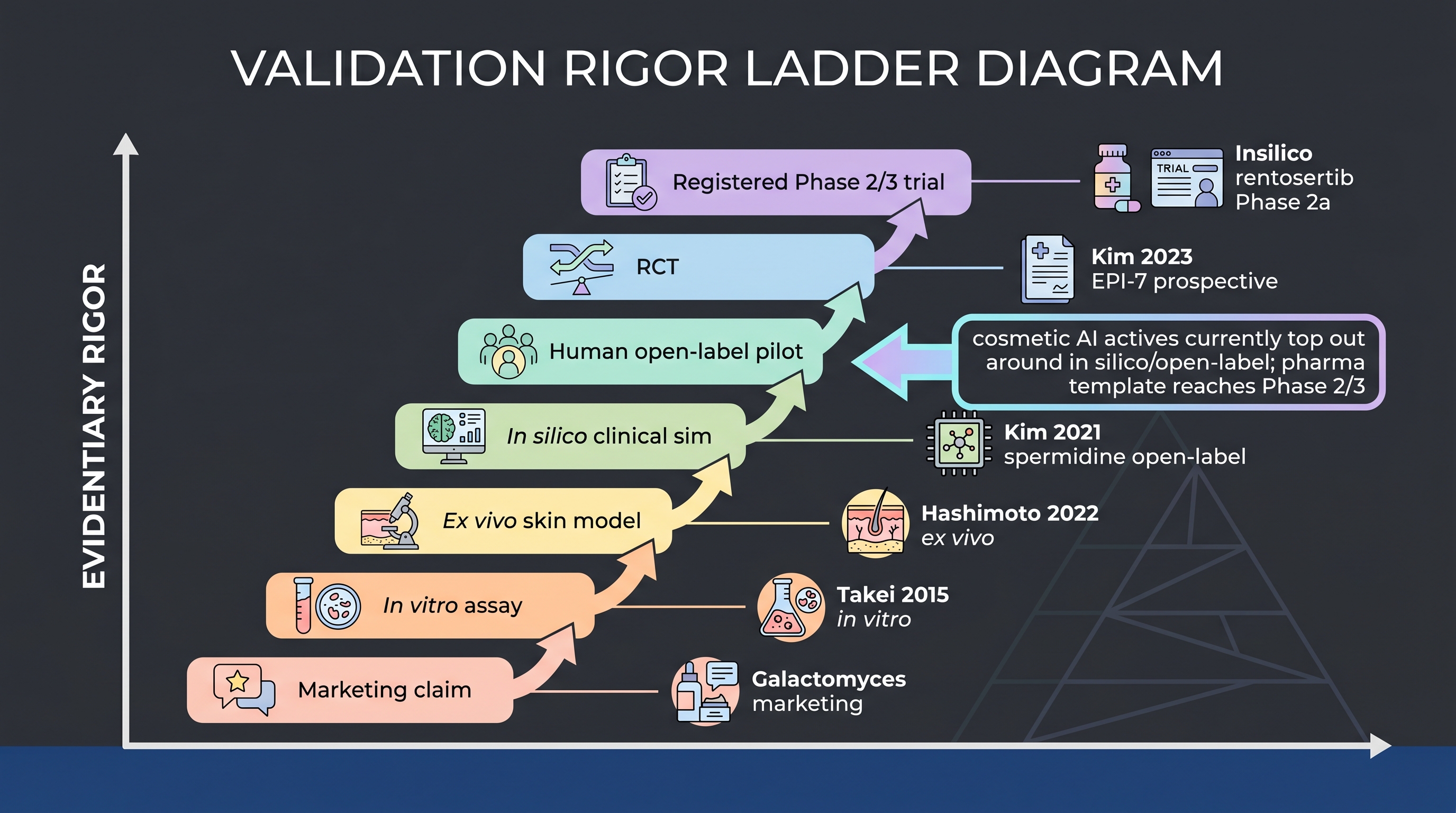
Chapter 4부터 Chapter 8까지는 AI 기반 설계 파이프라인을 단계적으로 쌓았다. 균주 트리아지, AlphaFold급 타겟 도킹, 마이크로바이옴-피부 상호작용 모델링, DBTL 합성생물학, 생성 모델·베이지안 제형 최적화. Chapter 8이 끝나는 시점에서 하나의 마이크로바이옴 화장품 후보 물질이 서류상으로는 존재한다. 예측된 타겟 결합, 예측된 생산 가능성, 예측된 제형 거동까지 모두 갖추고 있다. 그러나 그 어떤 예측도 아직 사람의 피부에는 닿지 않았다. 이 챕터는 닿는 단계에 관한 이야기다.
쟁점은 기술적이지 않다. 증거 기반이다. 제약 산업은 AI 설계 분자가 무작위 임상시험을 통과한 단일 사례를 이미 보유하고 있다 — Insilico의 rentosertib는 12주 시점에서 평균 강제폐활량(FVC) 변화 +98.4 mL 대 위약군 −20.3 mL로 Phase 2a를 통과했다 [23]. 같은 프로그램의 선행 Nature Biotechnology 논문은 타겟 발굴부터 IND 신청까지 약 30개월이 소요됐음을 문서화했다 [22]. 그러나 화장품 산업은 2026년 5월 현재 AI 설계 활성물질의 동급 임상 출판 사례가 영(0)이다 [11]. 한국의 COSMAX–단국대 축은 어느 단일 코퍼스 안에서든 가장 엄밀한 마이크로바이옴 화장품 임상 결과 — EPI-7 ferment filtrate 항노화 포스트바이오틱 [14]과 Streptococcus-spermidine 파이프라인 [13] — 을 보유하지만, 어느 쪽도 AI가 설계하지 않았다. 이 챕터가 다루는 검증 인프라가 바로 그 공백을 채울 도구다.
이 챕터의 정량적 핵심 3가지 1. 제약 템플릿 (rentosertib Phase 2a): 60 mg QD군 평균 FVC +98.4 mL 대 위약 −20.3 mL, 12주, 용량 의존적 추세. AI 설계 활성물질의 첫 임상 효능 readout [23]. 화장품 산업의 동급 사례는 영(0). 2. 한국 화장품 임상 레퍼런스 (EPI-7): 주름·탄력·수분·경피수분손실(TEWL) endpoint를 측정한 전향적 포스트바이오틱 국소 임상. 연세대-단국대-COSMAX BTI-HuNBiome 컨소시엄 [14]. 코퍼스 안에서 한국 마이크로바이옴 화장품 단일 출판물 중 가장 엄밀. 3. L'Oréal 공저 시스템 리뷰 (Haykal 2025): 74편 포함, 22개 RCT Level I, AI 설계 화장품 활성물질의 출판급 임상 readout은 0건 [11]. L'Oréal 자신의 저자들이 그 공백을 명명했다.
9.1 검증의 공백 — 왜 대부분의 AI 화장품 주장은 임상시험으로 끝나지 않는가
화장품 R&D와 제약 R&D는 서로 다른 증거 체제 아래 작동하며, 그 차이가 이어지는 거의 모든 현상을 설명한다. 새로운 의약품은 무작위·이중맹검·전향적 등록·통계적으로 충분한 검정력을 갖춘 임상시험을 통과해야 미국·EU·한국 시장에 진입할 수 있다. 새로운 화장품 활성물질은 그렇지 않다. 효능 입증은 마케팅 클레임과 안전성 도시에에 충분한 증거만 갖추면 되며, 둘 다 회사의 규제 부서가 평가하고 외부 이의 제기가 있을 때만 감사된다. 이 비대칭은 비윤리적인 것이 아니라, 국소·도포형 화장품 제품의 위험 프로파일이 전신 약물 노출보다 낮다는 사실을 반영한다. 그러나 그 결과는 예측 가능하다 — 화장품 산업이 동료심사 효능 임상시험을 출판할 인센티브는 약하다. AI가 설계한 화장품 활성물질이 성공하는 순간 그것은 즉시 사유 IP이자 마케팅 차별점이 되며, 회사는 특허를 출원하고 클레임 문안을 작성한다. New England Journal of Medicine에 보내지 않는다.
그 결과는 L'Oréal 자신의 시스템 리뷰가 정확하게 문서화한 그대로다 [11]. 화장품 유전체학 AI에 관한 74편의 연구가 포함됐고, 그 중 22편이 Level I 증거(무작위 대조 임상)에 도달했으나, AI가 설계한 화장품 활성물질을 동료심사 임상 readout까지 가져간 사례는 단 한 건도 없었다. Atallah 2025의 생체공학 마이크로바이옴 화장품 리뷰는 다른 각도에서 같은 결론에 도달한다 — 공학적 활성물질의 인용된 효능 클레임 대부분은 "동료심사 임상시험이 아닌 보도자료에 근거한다"고 명시한다 [3]. Di Guardo 2025 화장품 AI 리뷰는 화장품-프리바이오틱 AI가 "공공 데이터가 빈약해 거의 다뤄지지 않는다"고 적는다 [6]. 서로 다른 세 시각에서 출발한 세 리뷰가 동일한 공백으로 수렴한다.
이것이 책의 분석 레이어가 명명한 Gap 1이며, 세 챕터에서 하중을 받는다 — Chapter 5(AI 설계 도구는 준비됐다), 이 챕터(검증 인프라는 존재한다), Chapter 12(제안된 출판 템플릿). 이 공백은 기술적이지 않다. 경제적이며 문화적이다. 이 챕터의 나머지에서 다룰 모든 프레임워크 — ex vivo 모델, 임상 시뮬레이션, 디지털 바이오마커, EPI-7 연구, spermidine 파이프라인 — 은 오늘 단독으로 사용 가능하다. 빠진 것은 통합된 end-to-end 출판물이다.
화장품 산업은 이 자리에 와본 적이 있다. 1세대 발효 화장품(Pitera, 설화수, Galactomyces ferment filtrate)은 분자 수준 메커니즘 논문이 따라잡기 수십 년 전부터 마케팅됐다 — [24]는 Galactomyces ferment filtrate에 AHR 작용제로서의 첫 메커니즘을 부여했는데, Pitera의 상업 출시로부터 약 30년 후의 일이었다. [9]은 다시 7년 뒤 NRF2 축을 더했다. 역사적 패턴은 메커니즘이 마케팅을 수십 년 뒤따르는 형태였다. AI 변곡점은 바로 그 패턴을 뒤집겠다는 약속이다 — 메커니즘을 손에 쥔 채로 설계하고, 검증하고, 출판한 다음 클레임한다. 화장품 산업은 아직 그 패턴을 뒤집지 못했다. 이 챕터가 그 역전의 playbook이다.
9.2 Ex vivo 피부 모델 — 무엇을 재현하고 무엇을 재현하지 못하는가
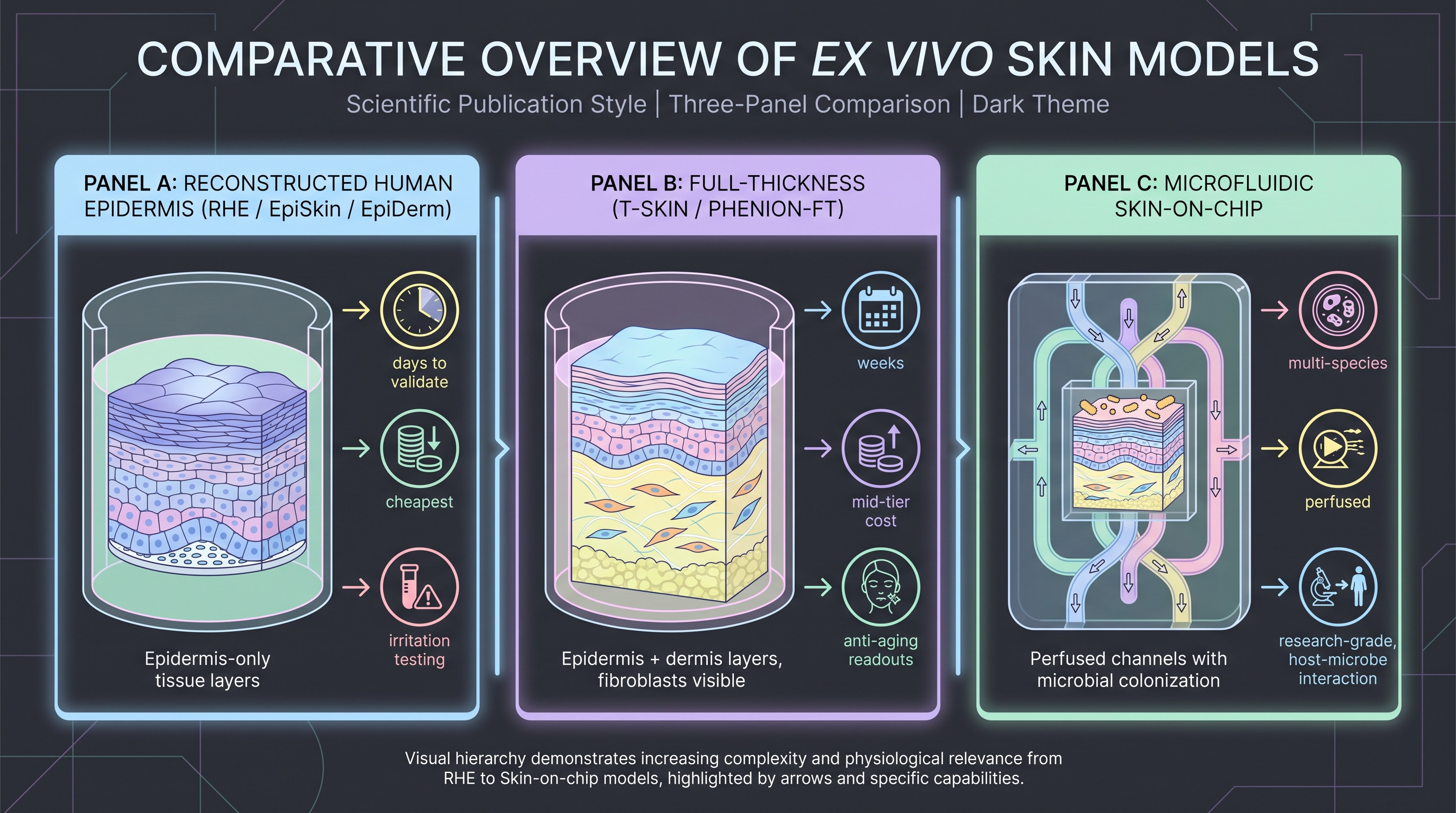
사람 피부가 아닌데 사람 피부에 가장 근접한 대체물은 재구성 피부 모델이다 — 케라티노사이트를 층상·분화된 표피 시트로 배양한 것이다. 두 개의 상업 플랫폼이 시장을 지배한다. EpiSkin(L'Oréal 계열)과 EpiDerm(MatTek, 2007년 표준화 물결 이후)이 재구성 인간 표피(reconstructed human epidermis, RHE) 조직으로, 자극·부식·감작 시험과 점차 효능 시험에까지 전 세계에서 사용된다. 두 플랫폼 모두 OECD 시험 가이드라인(부식 TG 431, 자극 TG 439) 아래 검증됐는데, 이는 화장품 회사가 동물 시험 대신 EU(2013년부터 화장품 동물시험 금지)·한국 그리고 점차 미국 규제 제출에 이 모델을 사용할 수 있다는 뜻이다. OECD 검증은 측정 시스템에 대한 자격이지 효능 자격이 아니다. 그러나 그 자격이 만들어낸 공급망 위에 그 다음의 효능 연구가 올라탔다.
RHE 위 생물학적 복잡도에 풀-시크니스 피부 모델(T-Skin, Phenion FT, EpiDerm-FT)이 있는데, 케라티노사이트 층 아래에 섬유아세포가 포함된 진피 컴파트먼트를 갖춘다. 이 모델은 순수 표피 모델이 다룰 수 없는 readout을 지원한다 — 콜라겐 합성, 진피-표피 접합 무결성, AlphaFold 유래 콜라겐 안정화 펩타이드와 같은 항노화 endpoint(Chapter 5). 단점은 풀-시크니스 모델 인서트당 비용이 RHE의 약 3–5배이고, 성숙에 더 오랜 시간(RHE의 1주 대비 2–3주)이 걸리며, 배치 간 변이가 작은 효과를 검출하기 위해 더 큰 반복 수를 요구한다는 점이다. 바로 이 경제적 마찰이 대부분의 AI 설계 화장품 후보를 풀-시크니스가 아니라 RHE로 밀어내고, 그것은 다시 ex vivo 단계에서 방어 가능한 메커니즘 깊이를 제한한다.
전선은 마이크로유체 skin-on-chip과 의도된 미생물 콜로나이제이션이다. 2025년 Nature Communications 하이드로겔 스캐폴드 피부 마이크로생태계 모델 [19]이 출판된 모범이다 — 피부 모사 스캐폴드 위에서 다종 미생물 군집을 안정적으로 유지하여 활성물질을 native commensal과 함께 체계적으로 시험할 수 있다. Verma 2024의 organoid biofilm 리뷰는 organoid 마이크로바이옴 통합 skin-on-a-chip을 "차세대 화장품 효능 시험에 필요"하다고 명시하며, 이는 Chapter 6의 디지털 트윈 모델이 가장 자연스럽게 접지되는 자리이기도 하다 [26]. 2026년 한계는 분명하다 — skin-on-chip은 여전히 연구 도구이지 산업 QC 도구가 아니다. 공급망은 분절돼 있고(각 랩이 자체 칩을 키우고, 교정 프로토콜이 표준화되지 않았으며, OECD 동급 검증이 아직 없다), 2026년 시점에서 AI 설계 화장품 활성물질을 위한 가장 깊은 ex vivo 검증은 현실적으로 skin-on-chip이지만, 그것만으로 규제급 readout이 만들어지지는 않는다.
이 모든 모델이 재현하지 못하는 것은 전체 면역학적 맥락이다. Ex vivo 모델은 기능적 적응 면역이 결여돼 있고, 전신 신경내분비 입력이 결여돼 있으며, 장벽 기능·마이크로바이옴 구성·면역 감시 사이의 만성 항상성 피드백 루프가 결여돼 있는데, 이는 [4]가 기반으로 확립한 축이다. EpiDerm IL-6 분석에서 우수 점수를 받은 AI 예측 항염 활성물질이 사람 사용에서 여전히 실패할 수 있는데, 모델이 포착하지 못한 인간 Th17–Treg 균형이 그것을 거부하기 때문이다. Ex vivo는 필요조건이지 충분조건이 아니다. 그리고 "필요"와 "충분" 사이의 간극이 정확히 in silico 임상 시뮬레이션과 사람 시험이 메워야 할 자리다.
L'Oréal 자신의 R&I 내부 리뷰는 이를 정직하게 인정한다 — 자사 분석 도구상자는 16S, shotgun, 메타볼로믹스, ex vivo 오가노타이픽 피부를 포함하며, 동시에 "낮은 바이오매스, 배치 효과, 샘플 수집 변이"가 지속되는 재현성 부담으로 명시된다 [8]. 업계 인사이더들은 이 논문을, 자원이 가장 풍부한 화장품 회사조차 학계 연구실과 동일한 ex vivo 한계에 부딪힌다는 가장 깨끗한 자기고백으로 읽는다.
9.3 In silico 임상 시뮬레이션 — 제약에서 옮겨온 PBPK와 QSP
제약 산업은 in silico 임상시험을 10년 이상 본격적으로 수행해왔다. 핵심 기술 스택은 두 층으로 나뉜다. 생리학 기반 약물동태학(PBPK)은 화합물이 각 컴파트먼트 — 장, 혈액, 장기 특이 조직 — 를 통과해 분포하는 양상을 ADME(흡수·분포·대사·배설) 매개변수의 기계론적 모델 아래 시뮬레이션한다. 정량 시스템 약리학(QSP)은 PBPK 위에 질병 메커니즘 모델 — 사이토카인 네트워크, 수용체 점유 동역학, 바이오마커 진행 — 을 더해, 후보 물질의 예측 혈장 농도가 예측 임상 endpoint로 번역되도록 한다. FDA는 의약품 규제 제출에서 PBPK와 QSP를 수용하고, EMA도 동일하다. 경구·주사 의약품 워크플로우는 성숙해 있다.
화장품 국소제에 대한 이식은 부분적이다. 국소 PBPK는 존재한다 — 1992년에 Potts–Guy 식이 화장품 화학자에게 분자량과 logP로부터 각질층 투과성을 예측하는 일차 원리 방법을 줬고, 현대 ML이 비선형 비히클·부형제 효과를 추가한다(Chapter 8). 화장품 특이 문헌에서 빈약한 것은 화장품 endpoint에 대한 QSP다 — 주름 깊이, 탄력, 수분. 그 이유는 화장품 endpoint가 의약품 endpoint처럼 바이오마커에 닻이 박혀 있지 않기 때문이다. IPF에 대한 제약 QSP 모델은 "FVC 변화"를 endpoint로 삼고, 약물 → TNIK 억제 → 섬유아세포 증식 → 콜라겐 침착 → 측정된 FVC라는 기계론적 사슬을 갖는다. "주름 개선"에 대한 화장품 QSP 모델은 동등한 엄밀성의 그 사슬을 결여한다. 주름 형태는 진피 콜라겐 품질, 진피-표피 접합 무결성, 수분, 표재 장벽 지형학의 복합 결과이며, 각각이 자기 자신의 불완전한 기계론적 모델을 가진다.
화장품 산업의 우회로는 가상 코호트 시뮬레이션이며, Chapter 8에서 제형 관점으로 살펴봤다. 같은 아키텍처가 임상 readout 시뮬레이션에도 기여한다. Unilever가 공개한 2,500명 AI 가상 코호트 [25]는 벤치 검증 전 제형을 사전 스크리닝하고, 개념적으로 동일 엔진이 사람 시험 전에 효능 결과를 사전 스크리닝할 수 있다. 미해결 문제는 교정이다. 가상 코호트는 구성상 실제 코호트의 평균 응답 분포를 맞출 수 있지만(실제 코호트로 학습됐기 때문), 새로운 민족·연령대·피부 타입으로의 일반화가 동작한다는 점을 독립적으로 검증할 수는 없다. 동료심사 화장품 문헌에는 제약 QSP 표준을 충족하는 출판된 가상 코호트 검증 연구가 아직 없다.
화장품 산업이 이를 배치할 때의 전이 템플릿은 이런 모양이다. (i) 방어 가능한 기계론적 사슬을 가진 화장품 endpoint를 식별한다 — 콜라겐 품질을 매개로 한 항노화가 가장 성숙한 후보이며, [13]이 spermidine-콜라겐 메커니즘 기준선을 제공한다. (ii) 후보 활성물질을 측정 가능한 중간자를 통해 endpoint와 잇는 QSP 형태의 모델을 만든다. (iii) 최종 임상이 사용할 동일 계측으로 작은 실제 사람 코호트에 대해 교정한다. (iv) 제형 × 용량 변종을 in silico로 사전 스크리닝하고, 생존자를 진행한다. (v) 등록된 전향적 임상을 수행하고 출판한다. 아래에 다룰 EPI-7 연구는 (iii)–(v)에 가장 가까운 기존 근사이지만, 가상 코호트를 사전 스크리닝에 공식적으로 사용하지는 않았다.
9.4 디지털 바이오마커 — 무엇이 측정으로 인정되는가
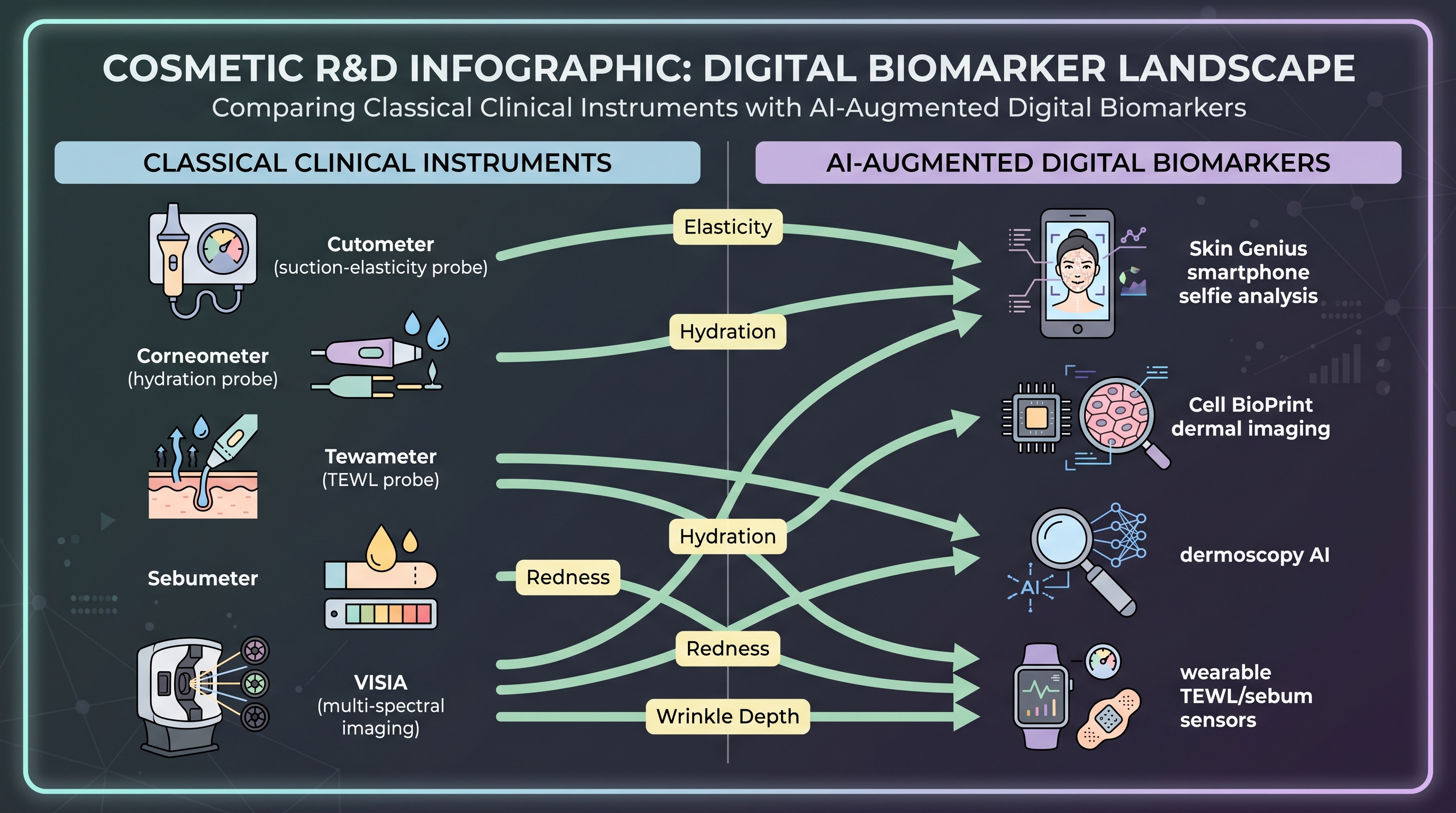
검증 사슬은 측정만큼만 신뢰 가능하다. 화장품 임상 연구는 역사적으로 표준 계측의 작은 집합을 사용해왔다 — cutometer(피부 탄력), corneometer(유전 상수를 이용한 수분), tewameter(경피수분손실), sebumeter(피지량), VISIA 영상(스펙트럼 채널을 가진 고해상도 사진). 방법론적 부담은 실재한다 — 계측기 간 변이, 조작자 효과, 환경 의존성(수분 측정의 비교성을 위해 실온 22°C, 상대 습도 40–50%가 필요). 화장품 임상시험 설계는 이 부담을 수십 년에 걸쳐 내재화했다. EPI-7 연구가 정확히 이 계측 세트를 사용했다 [14].
전선은 AI 증강 디지털 바이오마커다. 세 가닥이 중요하다. 첫째, 스마트폰 기반 피부 영상 AI. L'Oréal의 Skin Genius와 최근의 Cell BioPrint 플랫폼은 스마트폰급 영상에 합성곱 네트워크를 적용하여, 이전에 클리닉 계측이 필요했던 피부 속성 — 모공 가시성, 홍반, 색소 분포, 심지어 생물학적 피부 나이 — 을 예측한다. Skin Genius 진단 도구는 소매 채널과 소비자 앱을 통해 출시됐고 누적 추론 횟수가 1억을 넘었다 [17]. 동 시스템은 Modiface 및 체인 소매와의 파트너십을 통해 28개국으로 확장됐다 [16]. 셀링 포인트는 스마트폰 AI가 cutometer를 대체한다는 점이 아니다 — 대체하지 않는다 — 모든 소비자의 손에 일관된 종단 계측을 놓아, 클리닉 방문이 따라잡지 못하는 수주·수개월 단위의 in-home outcome 추적을 가능케 한다는 점이다.
둘째, 더모스코피 AI. 피부과 커뮤니티는 지난 10년 동안 흑색종, 기저세포암, 염증성 피부질환에 대한 합성곱 그리고 최근에는 Transformer 기반 분류기를 구축해왔다. 화장품 산업은 비의료 endpoint — 주름 깊이 분할, 피지선 모공 매핑, 홍반 국소화 — 에 동일 아키텍처를 채택하기 시작했다. 옥의 티는 데이터셋 편향이다. 출판된 더모스코피 AI 대부분이 더 밝은 Fitzpatrick 피부 타입에서 학습됐고, L'Oréal 공저 Haykal 리뷰는 "지리적 다양성이 제한되고, 어두운 phototype이 과소표현"되는 것을 화장품 AI의 구조적 재현성 실패 모드로 명시한다 [11]. Fitzpatrick I–III에서는 동작하고 IV–VI에서는 실패하는 디지털 바이오마커는 규제·윤리 관점에서 아직 디지털 바이오마커가 아니다.
셋째, 자동화된 TEWL·피지 센서. 웨어러블 패치와 벤치탑 디바이스가 측정 비용을 낮추고 측정 빈도를 높였다. 임상시험 설계에 대한 함의는, 한때 세 시점(기저, 4주, 12주)에서 측정되던 endpoint를 이제 연속적으로 측정할 수 있고, AI 요약 통계가 단일 판독을 대체한다는 것이다. 이는 피트니스 웨어러블이 영양 시험에 가져온 통계적 효율 향상과 같은 종류다 — ZOE PREDICT 코호트가 연속 혈당 모니터링으로 이를 활용한다 [2]. 화장품으로의 번역은 직접적이다. 어느 것도 AI 설계 활성물질 시험에 대규모로 배치된 적이 없는데, 다시 말하지만 그러한 시험이 출판된 적이 없기 때문이다.
종합이 중요하다 — 2026년에 AI 화장품 활성물질 임상시험을 출판할 측정 인프라는 존재한다. Cutometer, corneometer, tewameter, 더모스코피 AI, 스마트폰 영상, 자동 웨어러블 바이오마커, ex vivo 확증 분석 — 이 모두가 개별적으로 검증돼 있다. 빠진 것은 조율된 연구다.
9.5 EPI-7 — 한국 화장품 임상 레퍼런스
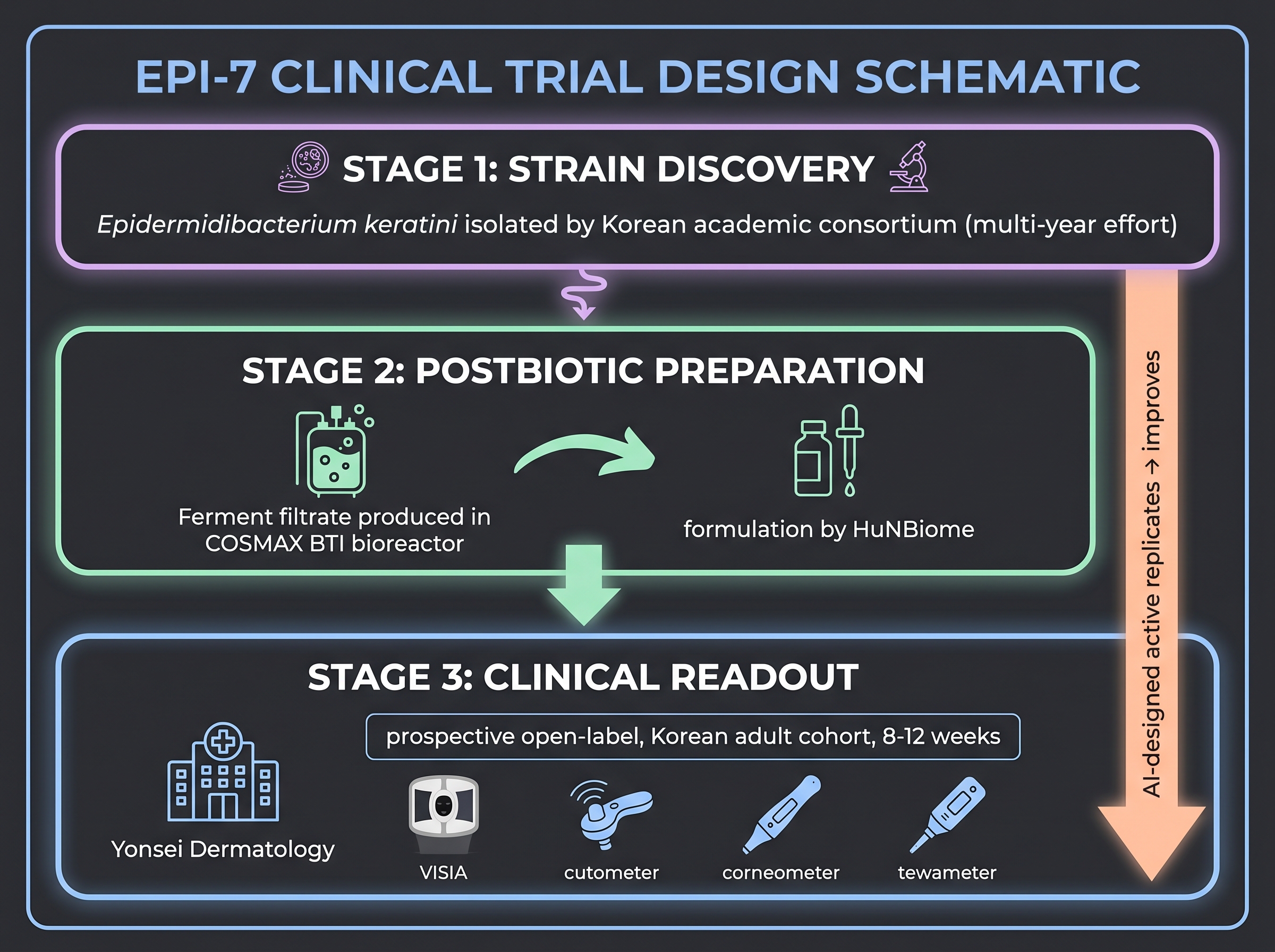
2023년 EPI-7 연구 [14]는 코퍼스에서 가장 엄밀하게 수행된 한국 마이크로바이옴 화장품 임상 readout이며, AI 화장품 활성물질 임상시험이 최소 엄밀성에서 어떤 모양이어야 하는지에 대한 유용한 템플릿이다. 시험 대상 물질은 Epidermidibacterium keratini — 같은 연세대–단국대–COSMAX BTI–HuNBiome 컨소시엄이 발굴한 신규 피부 유래 속(屬) — 에서 유래한 ferment filtrate 포스트바이오틱이었다. 이 협업의 구조 자체가 흥미롭다 — 연세대 피부과학교실이 임상 전문성(책임 저자 이주희·이영인 교수), 단국대가 유전체 분석학(한규동 교수), COSMAX BTI가 제조와 균주 뱅크, HuNBiome이 제형 개발을 담당했다.
시험 설계는 단순하다 — 한국 성인 코호트에 대한 전향적 국소 도포 연구로, 표준 계측 세트로 측정한 항노화 endpoint — VISIA 영상과 skin-replica 분석을 통한 주름 파라미터, cutometer로 탄력, corneometer로 수분, tewameter로 경피수분손실. 보고된 결과는 여러 endpoint에 걸친 기저 대비 유의한 개선이었다. 시험의 주된 한계는 이 투자 수준의 모든 화장품 연구가 짊어지는 것이다 — open-label, 단일군(위약 대조 없음), 단기간(전형적 8–12주). 이는 정직한 제약 조건이다 — 위약 대조 시험은 비용을 두 배로, 등록 부담을 세 배로 늘리고, 대부분의 화장품 활성물질은 그 추가 투자를 정당화할 상업적 기대를 만들어내지 않는다. EPI-7은 한국 마이크로바이옴 화장품 산업이 통상 출판하는 수준의 상단에 있다.
EPI-7을 AI 화장품 활성물질 출판 질문의 올바른 레퍼런스로 만드는 점은, 기저의 ferment filtrate가 AI 설계가 아니었다는 사실이다. 균주는 전통적인 미생물 분리·분류로 발견됐고, 고전적 미생물학으로 캐릭터라이즈됐으며, 표준 방법으로 발효됐고, 표준 화장품 임상 프로토콜로 시험됐다. 시험은 AI가 부재한 상태의 검증 사슬이다. 이 책의 주장은 AI 설계 활성물질이 적어도 이 엄밀성 — 같은 계측 세트, 같은 통계 분석, 같은 출판 매체, 같은 저자 컨소시엄 구조 — 을 목표로 해야 하며, 가능하면 위약 대조 군을 더해 그것을 넘어서야 한다는 것이다. 그를 위한 기술 스택은 2024년부터 준비돼 있다.
미묘한 지점 — EPI-7은 또한 묵시적으로 균주 수준 연구의 가치를 입증한다. Epidermidibacterium keratini 속은 한국 컨소시엄이 기술하기 전까지 출판된 분류에 존재하지 않았다. 시험은 원본 균주 발굴, in vitro 메커니즘 연구, 그리고 수년이 걸린 자체 발효 개발의 하류에 위치한다. 이것이 정확히 seed.md와 Chapter 3의 AI는 예측하고, culture는 검증한다는 비대칭이다 — AI 예측 레이어는 무로부터 부트스트랩될 수 없다. 예측 대상이 될 균주 코퍼스와 측정 인프라가 필요하다. EPI-7의 임상 성공은 AI가 만들지 않은 culture collection까지 거슬러 올라간다.
9.6 COSMAX–단국대 spermidine 파이프라인 — "잘 된 사례"의 모습
EPI-7이 임상 readout 템플릿이라면, [13] spermidine 연구는 end-to-end 파이프라인 템플릿이다. 한국의 단일 산학 컨소시엄(COSMAX BTI + GIST + Genome and Company + KIST + 경희대) 내부에서 예측–설계–검증의 전체 사슬이 실행된 가장 깨끗한 출판 사례이며, Nature 패밀리의 오픈 액세스 동료심사 저널인 Communications Biology에 출판됐다.
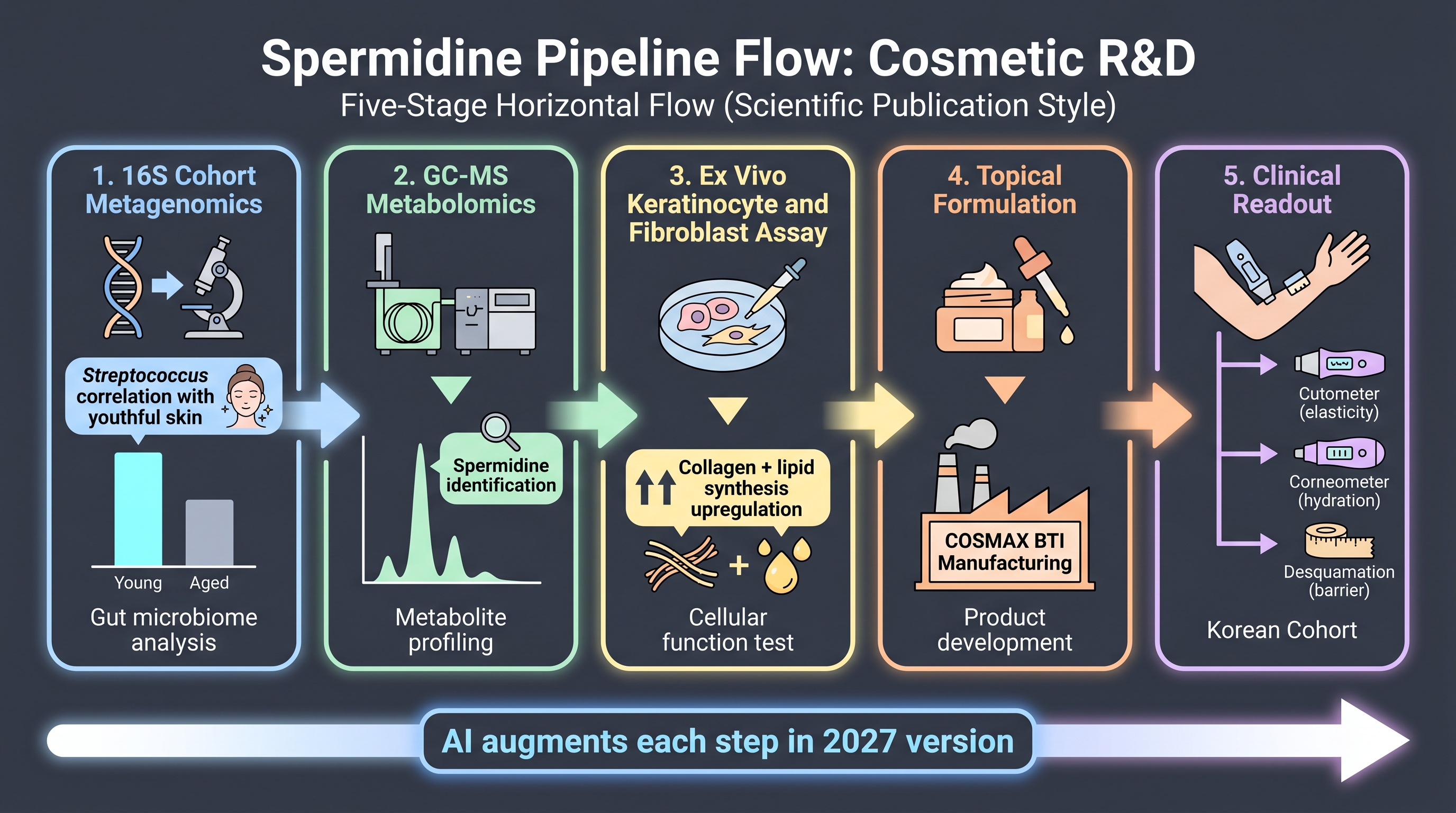
파이프라인. (i) 메타지노믹스로 균주 발굴: 한국 피부 코호트의 16S 시퀀싱이 Streptococcus 종(S. pneumoniae, S. infantis, S. thermophilus)을 더 어리고 더 탄력 있는 피부에 풍부한 균으로 식별했다. 발굴 레이어는 상관관계 메타지노믹스 — 책의 Chapter 4가 AI 친화적으로 프레임화한 동일 아키텍처가, 여기서는 고전적 통계 방법으로 실행됐다. (ii) GC-MS 메타볼로믹스로 대사체 식별: spermidine이 탄력 연관성을 그럴듯하게 설명하는 Streptococcus 분비 대사체 후보로 부상했다. (iii) Ex vivo 세포 시스템에서 메커니즘 검증: spermidine을 처리한 노화 케라티노사이트와 섬유아세포가 콜라겐과 지질 합성을 전사체 수준에서 상향 조절함을 보였다. (iv) 사람 도포에서 국소 효능: spermidine 함유 국소 제형이 임상 연구에서 탄력(cutometer), 수분(corneometer), 박리(desquamation)를 개선했다.
이것은 16S 상관관계에서 측정된 임상 endpoint까지 다섯 단계의 사슬이며, 2021년에 출판됐고, 한국 컨소시엄에 의해, EPI-7 시험이 2년 후 사용한 것과 동일한 계측 세트로 수행됐다. 저자들은 한계에 대해 정직하다 — 상관관계 메타지노믹스는 in vivo 인과를 증명하지 못하고, 임상 단계는 위약 없는 open-label이었으며, spermidine 단독과 Streptococcus 전체 secretome 사이의 메커니즘 분리는 불완전하다. 이 한계 각각은 정확히 AI 기반 버전의 파이프라인이 다룰 수 있는 항목이다 — AI는 후보 대사체를 대규모로 사전 스크리닝하여 spermidine이 지배적 활성물질임을 논증할 수 있고(메커니즘 분리), AI 가상 코호트 사전 스크리닝이 위약 대조 군의 모집 부담을 줄일 수 있으며(통계 검정력), AlphaFold급 타겟 도킹이 spermidine이 어느 숙주 타겟과 engage하는지 논증할 수 있다(메커니즘). 2021 파이프라인은 출판되기 위해 AI를 필요로 하지 않았다. AI-augmented 2027 버전은 동일 골격 위에서 더 엄밀하게 출판할 것이다.
이것이 seed.md에서 AI는 예측하고, culture는 검증한다가 의미하는 바다. Kim 2021 파이프라인은 화장품 마이크로바이옴 효능 출판의 작동하는 템플릿이다. AI 레이어는 가산적이지 대체적이지 않다.
9.7 제약 전이 템플릿 — 운영 목표로서의 rentosertib
화장품 산업이 아직 복제하지 못한 전이 템플릿은 Insilico Medicine의 rentosertib(ISM001-055) 프로그램이다. Nature Biotechnology 논문 [22]은 타겟 식별부터 IND 신청까지 약 30개월에 걸친 프로그램을 문서화한다 — Insilico의 PandaOmics 플랫폼이 TNIK을 새로운 IPF 타겟으로 식별했고, Chemistry42 생성 화학이 소분자를 설계했으며, in vitro·in vivo 검증이 뒤따랐고, IND-enabling 독성학이 통과됐으며, Phase 0/1이 보고됐다. 후속 Nature Medicine 논문 [23]은 Phase 2a 무작위 이중맹검 결과를 보고한다 — 60 mg QD군 평균 FVC +98.4 mL 대 위약 −20.3 mL, 12주, 용량 의존적 추세, 안전성 프로파일이 Phase 3 진행을 지지함. 2025년 Insilico는 그 해 최대 규모의 홍콩 바이오테크 IPO로 홍콩 증권거래소에 상장하여 Phase 3 확장과 30개 이상의 프로그램 파이프라인을 자본화했다 [Insilico, 2025-HKEX].
화장품 활성물질이 FDA IND를 거치지 않는다는 점을 감안할 때, 화장품 산업의 동급 사례는 어떤 모양일까? 종착점 출판물은 다음 같은 모양의 Communications Biology 또는 British Journal of Dermatology 논문일 것이다. (a) AlphaFold급 타겟 예측(Chapter 5)이 정의된 화장품 관련 숙주 타겟(콜라겐 안정화, MMP 억제, AHR 조절)에 대한 마이크로바이옴 유래 대사체나 펩타이드 후보를 산출한다. (b) 합성생물학 대량 생산(Chapter 7)이 용량 조절된 국소 제형을 가능케 한다. (c) RHE 또는 풀-시크니스 모델에서 타겟 결합 바이오마커를 직접 측정한 ex vivo 메커니즘 검증. (d) 표준 화장품 계측(cutometer, corneometer, tewameter, VISIA)과 시험 등록을 갖춘 무작위·이중맹검·위약 대조 국소 임상시험. (e) 효과 크기, 탈락, 이상반응에 대한 정직한 보고. 이를 수행할 기술은 존재한다. 어느 메이저에도 그를 위한 경제적 인센티브가 아직 존재하지 않을 뿐이다.
가장 그럴듯하게 그러한 시험을 처음 출판할 화장품 산업 후보는 Big-4 서구 메이저가 아니다. (a) AI 설계를 전단에 추가하여 EPI-7 또는 spermidine 파이프라인을 확장하는 한국 컨소시엄, (b) 정의된 메커니즘 활성물질을 가지면서 동료심사 증거에 보상하는 마케팅 전략을 가진 합성생물학 스타트업(Geltor의 PrimaColl GRAS 레터 [7]가 섭취형 동급 사례이며, 국소 동급 사례는 아직 신청되지 않음), 또는 (c) AI 유래 클레임에 대한 EU 화장품 규제(CPR) 강화를 예상하여 압박받는 EU 중견 회사 [6] 중 하나일 것이다. 책의 예측(분석 레이어의 Gap 1)은 첫 출판 사례가 Big-4 메이저가 아니라 한국이나 중견 EU 출처에서 2027–2028년에 나오리라는 것이다.
이것이 한국 R&D 기획자에게 중요한 이유는 경쟁적이다. 출판급 임상 readout은 마케팅급 클레임이 따라잡지 못하는 방어 가능한 시장 차별점이다. 첫 AI 설계 화장품 활성물질 임상시험을 출판하는 한국 회사는 그 분야 역사의 영구적 한 조각을 갖게 된다. 그를 수행하는 비용 — 마케팅 대안의 비용 대비 — 은 Chapter 12가 기획 청사진에서 다시 다룰 질문이다.
9.8 공백 — 임상에 도달한 AlphaFold 유래 화장품 활성물질은 0건
이 절은 책의 중심 긴장을 가능한 한 깨끗하게 명명한다. AI 설계 도구상자는 2024년에 commodity 단계에 도달했다 — AlphaFold 3 [1], Boltz-1 [27], Chai-1 [5], ESM3 [10], RoseTTAFold-AllAtom [15], 그리고 6억 1,700만 개 이상의 예측 구조를 담은 ESMFold 유래 Metagenomic Atlas [18]가 화장품 활성물질 universe에 대한 단백질 구조·상호작용 예측을 commodify했다. 합성생물학은 공학적 활성물질을 대량 생산한다(Chapter 7). Ex vivo·임상 계측 인프라는 존재한다(9.2절, 9.4절). 한국 산학 컨소시엄은 코퍼스에서 가장 깨끗한 화장품 마이크로바이옴 임상 연구를 출판했다(9.5절, 9.6절). 제약 템플릿은 AI 설계 활성물질이 무작위 시험을 통과할 수 있음을 입증한다(9.7절).
그러나 2026년 5월 현재 출판된 화장품 문헌은 AlphaFold 유래(또는 일반적으로 AI 설계) 화장품 활성물질의 동료심사 임상시험을 0건 포함한다. Haykal 2025 PRISMA 리뷰가 L'Oréal R&I 저자 네트워크 내부에서 이 부재를 확인했다 [11]. Atallah 2025 생체공학 마이크로바이옴 화장품 리뷰는 대부분의 효능 클레임이 보도자료에 의존한다고 적는다 [3]. Di Guardo 2025 화장품 AI 리뷰는 AI 유래 효능 클레임 규제 프레임워크의 부재를 명시한다 [6]. 독립적인 세 리뷰, 일관된 하나의 발견.
Chapter 12에 대한 함의는 운영적이다. 책의 기여는 이 공백을 기술하는 데 그치지 않고, 그것을 닫을 것이 무엇인지 지정하는 것이다 — 최소 가용 화장품 AI 활성물질 출판 템플릿(endpoint 정의, 현실적 효과 크기 아래의 표본 크기, 맹검 전략, 계측 선택, 통계 분석 계획, 사전 등록 매체). Chapter 12는 이를 한국 R&D 기획자와 중견 글로벌 회사를 위한 세 가지 작동 가능한 청사진 중 하나로 다시 다룬다.
이 공백은 또한, 솔직히, 기회 벡터다. 먼저 출판하는 회사가 그 분야의 역사적 닻을 소유한다. 비용 — 잘 설계된 RCT 하나, 동료심사 출판, 코호트 크기와 기간에 따라 약 50만–100만 달러 수준의 계측 비용 — 은 같은 회사가 단일 캠페인에 쓰는 마케팅 예산에 비하면 작다. 아무도 하지 않는 이유는 비용이 아니다. 화장품 R&D가 과연 이 엄밀성으로 출판해야 하는가에 대한 문화적 관성이다. 책의 주장은 이 문화를 가장 먼저 바꾸는 회사들이 향후 10년 화장품 R&D의 외부 신뢰성을 정의할 것이라는 점이다.
9.9 규제 고려 — 짧은 예고
전체 규제 처리는 Chapter 12의 책임이다. 이 챕터의 논증을 위해 세 포인트가 중요하다.
FDA 화장품 vs OTC 약품 경계. 미국에서 화장품은 의도된 사용("청결, 미화, 매력 증진, 또는 외관 변경")으로 정의되며, FDCA 601조 아래에서 사전 시장 승인 요구가 없다. OTC 약품 — 자외선 차단제, 비듬 샴푸, 여드름 치료제 — 은 모노그래프를 준수하거나 NDA 승인을 받아야 한다. AI 설계 화장품 활성물질은 기본적으로 화장품 범주에 속하며, 그래서 임상시험이 요구되지 않는다. 그러나 활성물질이 치료적 영역에 접근하는 클레임(여드름, 아토피피부염, 습진)을 만들기 시작하면 OTC 약품 규제로 경계를 넘어가게 되며, 거기서 임상 증거가 의무화된다. Gallo 랩의 ShA9 S. hominis 프로그램 [20]은 아토피피부염에 대한 자가 박테리오테라피로 OTC 화장품이 아닌 FDA-IND 약품 경로를 명시적으로 선택했고, 그 전략적 선택은 화장품 경로 경쟁자가 직면하지 않는 임상 증거 요건을 동반했다.
한국 MFDS 기능성 화장품 클레임. 대한민국은 중간 규제 계층 — 기능성 화장품 — 을 보유하며, 이는 특정 클레임(미백, 항노화, 자외선 차단)에 대해 일반 화장품 입증 위, 약품 입증 아래의 효능 입증을 요구한다. EPI-7 [14]과 spermidine 연구 [13]에서 사용된 한국 계측 세트는 MFDS 기능성 화장품 입증 요건에 맞춰 교정된 것이다. 이것이 한국 마이크로바이옴 화장품 임상 연구가 서구 화장품 동급 대비 더 높은 엄밀성으로 출판되는 한 이유다 — MFDS 입증이 선택이 아니라 강제 함수다.
EU 화장품 제품 규제(CPR). EU의 2009 CPR과 부속서 I 아래의 안전성 평가 요건은 글로벌 화장품 프레임워크 중 가장 강력한 사전 시장 입증 체제를 만든다. 입증은 제품 정보 파일(PIF)에 문서화돼야 한다. AI 유래 효능 클레임은 전통적 클레임과 동일한 문서화 요구에 속하지만, EU CPR이 AI 예측이 입증 사슬에 어떻게 진입하는지에 관한 가이드는 아직 없다. [6]는 EU CPR 가이드가 2027년까지 나올 것으로 예상한다. Geltor PrimaColl GRAS 레터 [7]는 AI 또는 합성생물학 유래 활성물질이 규제 인정을 받은 가장 가까운 기존 미국 선례이지만, 섭취형에 한정된다.
Chapter 12는 위 각각을 운영 디테일과 함께 발전시키며, AI 유래 화장품 활성물질에 특화된 재현성 체크리스트와 2027–2030년을 위한 출판 템플릿을 제안한다.
9.10 Open Questions
- 검증 엄밀성 escalation — 첫 출판된 AI 설계 화장품 활성물질 임상시험은 한국 컨소시엄(EPI-7 / spermidine을 AI 전단으로 확장), 합성생물학 스타트업(Geltor 이후의 국소 동급 사례), 또는 규제 압박을 받는 EU 회사 중 어디에서 나올 것인가? 책의 작업 가설 예측은 2027–2028년 한국 또는 중견 EU. 대안은 Big-4 내부 데이터가 동료심사에 영원히 도달하지 않는 것이다.
- 디지털 바이오마커 표준화 — 스마트폰 기반 피부 영상 AI(Skin Genius, Cell BioPrint)가 phototype과 디바이스 전반에 걸쳐 표준화되어 규제급 종단 바이오마커로 기능할 수 있는가? 현재 한계는 Fitzpatrick I–III 과대표현 [11]이며, 이는 해결 가능하지만 의도된 코호트 확장을 요구한다.
- 마이크로바이옴 종단 데이터 인프라 — 미생물 콜로나이제이션이 포함된 ex vivo skin-on-chip이 현실적으로 얼마나 오래 유지될 수 있는가? 2주? 3개월? 안정 콜로나이제이션 윈도우가 길수록 readout의 임상적 관련성이 커지지만, 현재 어느 상업용 칩도 안정한 다종 군집 유지를 수 주 이상 넘기지 못한다.
- 임상 효능에 대한 가상 코호트 교정 — Unilever의 AI 가상 코호트 아키텍처 [25]가 규제 감사를 통과할 수준으로 교정될 수 있는가? 출판된 검증 연구가 아직 없으며, 이는 화장품 임상 시뮬레이션에 대해 가장 결과를 좌우하는 단일 방법론 질문이다.
- 기능성 화장품 vs 코스메슈티컬 규제 경계 — AI 설계 활성물질이 치료적 효과 크기에 접근하면서 규제 당국이 화장품/약품 경계를 강화할 것인가? Gallo S. hominis 프로그램은 분야가 분화될 것임을 시사한다 — 효능급 활성물질은 약품 또는 기능성 화장품 경로로 이동하고, 마케팅급 활성물질은 일반 화장품에 남는다. 선은 움직일 것이며, 질문은 어느 방향으로 어떤 속도로 움직이는가다.
참고문헌
- Abramson, J., Adler, J., Dunger, J. et al. (2024). Accurate structure prediction of biomolecular interactions with AlphaFold 3. Nature 630, 493–500.
- Asnicar, F., Berry, S. E., Valdes, A. M. et al. (2021). Microbiome connections with host metabolism and habitual diet from 1,098 deeply phenotyped individuals. Nature Medicine 27, 321–332.
- Atallah, R., Ahmed, A., Shams, M. et al. (2025). Bioengineered Skin Microbiome — Cosmetic Ingredient Landscape and Regulatory Considerations. Cosmetics 12(5):205.
- Belkaid, Y. and Tamoutounour, S. (2014). The compartmentalized and systemic control of tissue immunity by commensals. Nature Immunology 15, 646–653.
- Chai Discovery (2024). Chai-1 — Decoding the Molecular Interactions of Life. Technical report, Sep 2024. [Chai Discovery, 2024]
- Di Guardo, A., Trovato, F., Cantisani, C. et al. (2025). Artificial Intelligence in Cosmetic Formulation: Predictive Modeling for Safety, Tolerability, and Regulatory Perspectives. Cosmetics 12(4):157.
- Geltor (2025). Geltor PrimaColl receives FDA GRAS "no questions" letter. Geltor press, October 2025. [Geltor, 2025]
- Gueniche, A., Perin, O., Bouslimani, A. et al. (2022). Advances in Microbiome-Derived Solutions and Methodologies Are Founding a New Era in Skin Health and Care. Pathogens 11(2):121.
- Hashimoto-Hachiya, A., Furue, M., Tsuji, G. (2022). Galactomyces Ferment Filtrate Potentiates an Anti-Inflammaging System in Keratinocytes. Journal of Clinical Medicine 11(22):6691. [Hashimoto et al., 2022]
- Hayes, T., Rao, R., Akin, H. et al. (2025). Simulating 500 million years of evolution with a language model (ESM3). Science 387, 850–858.
- Haykal, D., Flament, F., Amar, D. et al. (2025). Cosmetogenomics unveiled: a systematic review of AI, genomics, and the future of personalized skincare. Frontiers in Artificial Intelligence 8:1660356.
- Insilico Medicine (2025). Insilico Medicine lists on Hong Kong Stock Exchange — largest HK biotech IPO of 2025. Insilico press, 2025. [Insilico, 2025-HKEX]
- Kim, G., Kim, M., Kim, M. et al. (2021). Spermidine-induced recovery of human dermal structure and barrier function by skin microbiome. Communications Biology 4:231.
- Kim, J., Lee, Y. I., Mun, S. et al. (2023). Efficacy and Safety of Epidermidibacterium Keratini EPI-7 Derived Postbiotics in Skin Aging: A Prospective Clinical Study. International Journal of Molecular Sciences 24(5):4634.
- Krishna, R., Wang, J., Ahern, W. et al. (2024). Generalized biomolecular modeling and design with RoseTTAFold All-Atom. Science 384, eadl2528.
- L'Oréal (2024). L'Oréal Beauty Tech leadership at VivaTech 2024 — AI Skin Genius, Modiface, microbiome direction. L'Oréal press, May 2024. [L'Oréal, 2024]
- L'Oréal R&I (2024). The Future of Cosmetics Is Playing Out In The Microbiome. L'Oréal R&I editorial, 2024. [L'Oréal R&I, 2024]
- Lin, Z., Akin, H., Rao, R. et al. (2023). Evolutionary-scale prediction of atomic-level protein structure with a language model. Science 379, 1123–1130.
- Microecology consortium authors (2025). Hydrogel-based scaffold in vitro skin microecology model supporting stable multi-species microbiota. Nature Communications (2025). [Microecology et al., 2025]
- Nakatsuji, T., Chen, T. H., Narala, S. et al. (2017). Antimicrobials from human skin commensal bacteria protect against Staphylococcus aureus and are deficient in atopic dermatitis. Science Translational Medicine 9, eaah4680.
- Nakatsuji, T., Hata, T. R., Tong, Y. et al. (2021). Development of a human skin commensal microbe for bacteriotherapy of atopic dermatitis. Nature Medicine 27, 700–709.
- Ren, F., Aliper, A., Chen, J. et al. (2024). A small-molecule TNIK inhibitor (ISM001-055 / rentosertib) discovered via end-to-end generative AI from target identification to Phase 1. Nature Biotechnology.
- Ren, F., Zhavoronkov, A. et al. (2025). A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine, May 2025.
- Takei, K., Mitoma, C., Hashimoto-Hachiya, A. et al. (2015). Galactomyces Ferment Filtrate Prevents T-Helper 2-Mediated Reduction of Filaggrin in an Aryl Hydrocarbon Receptor-Dependent Manner. Journal of Cutaneous Pathology.
- Unilever Beauty & Wellbeing R&D (2025). How Unilever's pioneering skin microbiome research is shaping product innovation. Unilever news, 2025. [Unilever, 2025]
- Verma, A., Singh, V. et al. (2024). Organoid and biofilm models for skin and lung microbial infection research. npj Biofilms and Microbiomes (2024).
- Wohlwend, J., Corso, G., Passaro, S. et al. (2024). Boltz-1 — Democratizing Biomolecular Interaction Modeling. bioRxiv preprint, Nov 2024.