Chapter 3: NGS와 메타지노믹스 — 미생물을 읽는 기술의 진화
이 챕터를 왜 읽는가. 마이크로바이옴 화장품이 발효 시대에서 데이터 시대로 넘어온 가장 큰 이유는 단 하나, "미생물을 읽는 비용"이 30년 만에 백만 분의 일로 떨어졌기 때문이다. 그런데 같은 시간 동안 "미생물을 키우는 기술"도 사라지지 않았다. 오히려 culturomics라는 이름으로 부활해 시퀀싱과 짝을 이루고 있다. 이 챕터는 16S부터 long-read까지의 읽기 기술과 culturomics 부활을 한 호흡으로 정리하고, Brief A의 핵심 질문 — "그럼 분리·동정·배양 같은 기초 연구는 이제 다 구식이 됐나?" — 에 책의 입장을 명확히 밝힌다. 답은 아니다. 보완 관계다. AI는 예측하고, 배양은 검증한다.
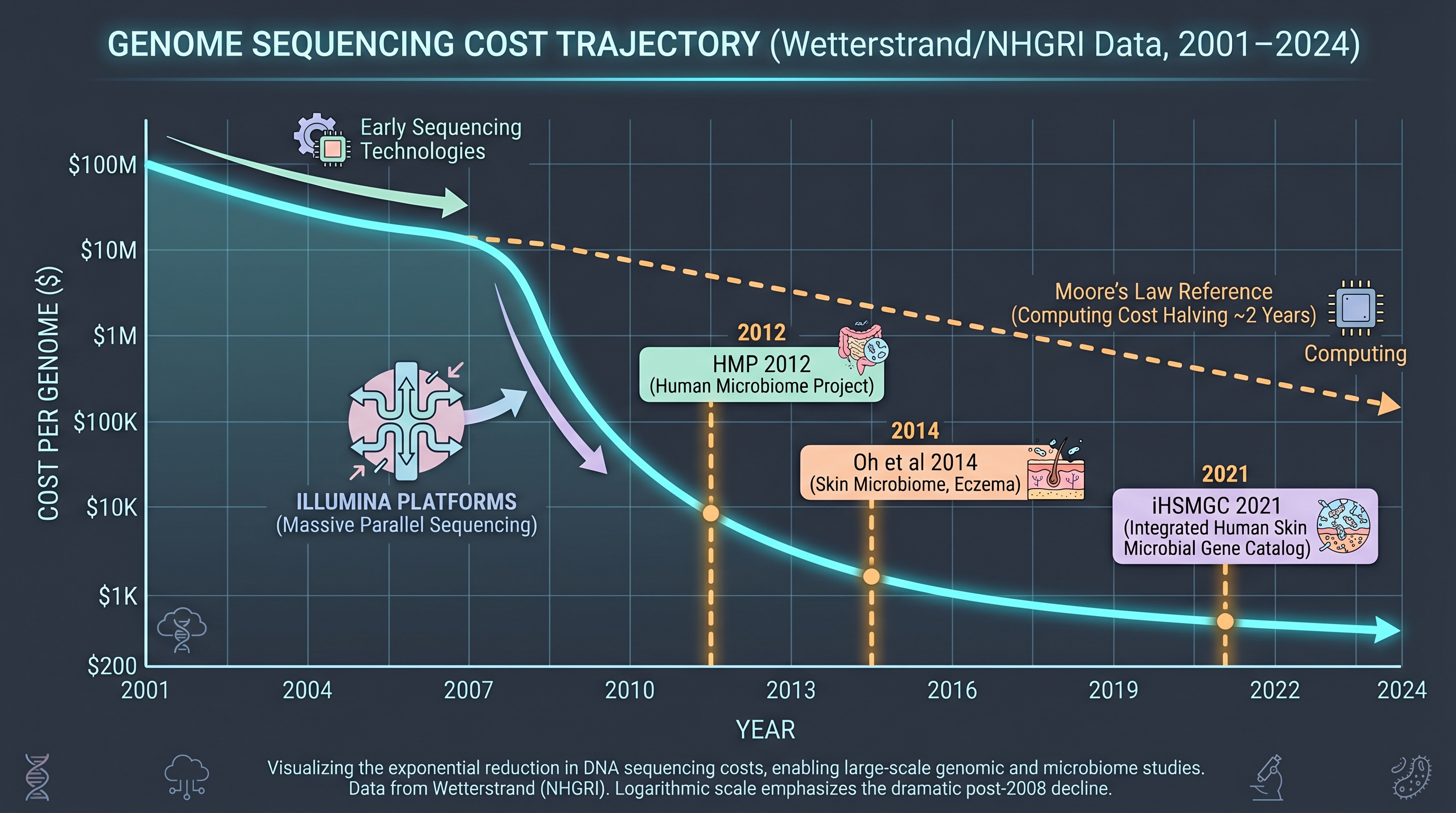
정량적 핵심 3가지. - 사람 한 명 분량의 게놈을 읽는 비용은 2001년 $100M에서 2024년 $200 수준으로 약 5×10⁵배 감소했다 — 이 곡선이 마이크로바이옴 산업화의 토대다. - L'Oréal·Unilever·COSMAX 같은 산업 컨소시엄은 수만~수십만 샘플의 자체 코호트를 보유하지만, 공공 reference인 HMP는 피부 부위가 3곳뿐이고 iHSMGC는 동아시아 코호트에서 HMP가 놓친 ~45%의 유전자를 발견했다 — 데이터 비대칭은 그 자체로 챕터 4·12의 출발선이다. - Culturomics는 2018년까지 사람 미생물에서 1,000종 이상의 미배양 균을 회수했다 — 이 중 피부 특이적 카탈로그는 아직 만들어지지 않았으며, 이것이 책의 핵심 gap 중 하나다.
3.1 왜 "읽기"가 필요했나 — 현미경에서 게놈까지
피부에 사는 미생물을 처음 본 것은 17세기 안톤 판 레이우엔훅(Antonie van Leeuwenhoek)의 자가 제작 현미경이었다. 이후 19세기 코흐(Robert Koch)와 파스퇴르의 배지 시대를 거치면서 우리는 한 균을 분리하고, 키우고, 표현형을 보는 데 익숙해졌다. 발효 화장품은 이 시대의 유산이다 (Chapter 1). 그러나 1990년대 후반에 들어 두 가지가 명확해졌다.
첫째, 피부에 사는 미생물 대부분은 표준 배지에서 자라지 않는다 — 소위 great plate count anomaly. 둘째, 같은 종이라도 균주(strain)에 따라 효능과 병원성이 완전히 다르다. 16S rRNA 유전자라는 분류학적 시계가 발견되고 그 시퀀싱이 가능해지면서 비로소 "키우지 않고 본다"는 길이 열렸다.
이 흐름의 결정적 인프라는 두 가지였다. 하나는 차세대 시퀀싱(Next-Generation Sequencing, NGS) 비용 곡선 — 2001년 한 사람의 게놈을 읽는 데 $100M이 들었지만 2024년에는 $200 수준이다. 다른 하나는 [5] QIIME 같은 오픈소스 분석 파이프라인이 표준이 되어 누구나 같은 방법으로 데이터를 처리할 수 있게 된 것이다. QIIME 원논문은 인용수 4만 회를 넘겼으며, 후속 [2] QIIME 2는 사실상 학계 표준이다.
3.2 16S rRNA amplicon — 가성비 좋은 첫 번째 망원경
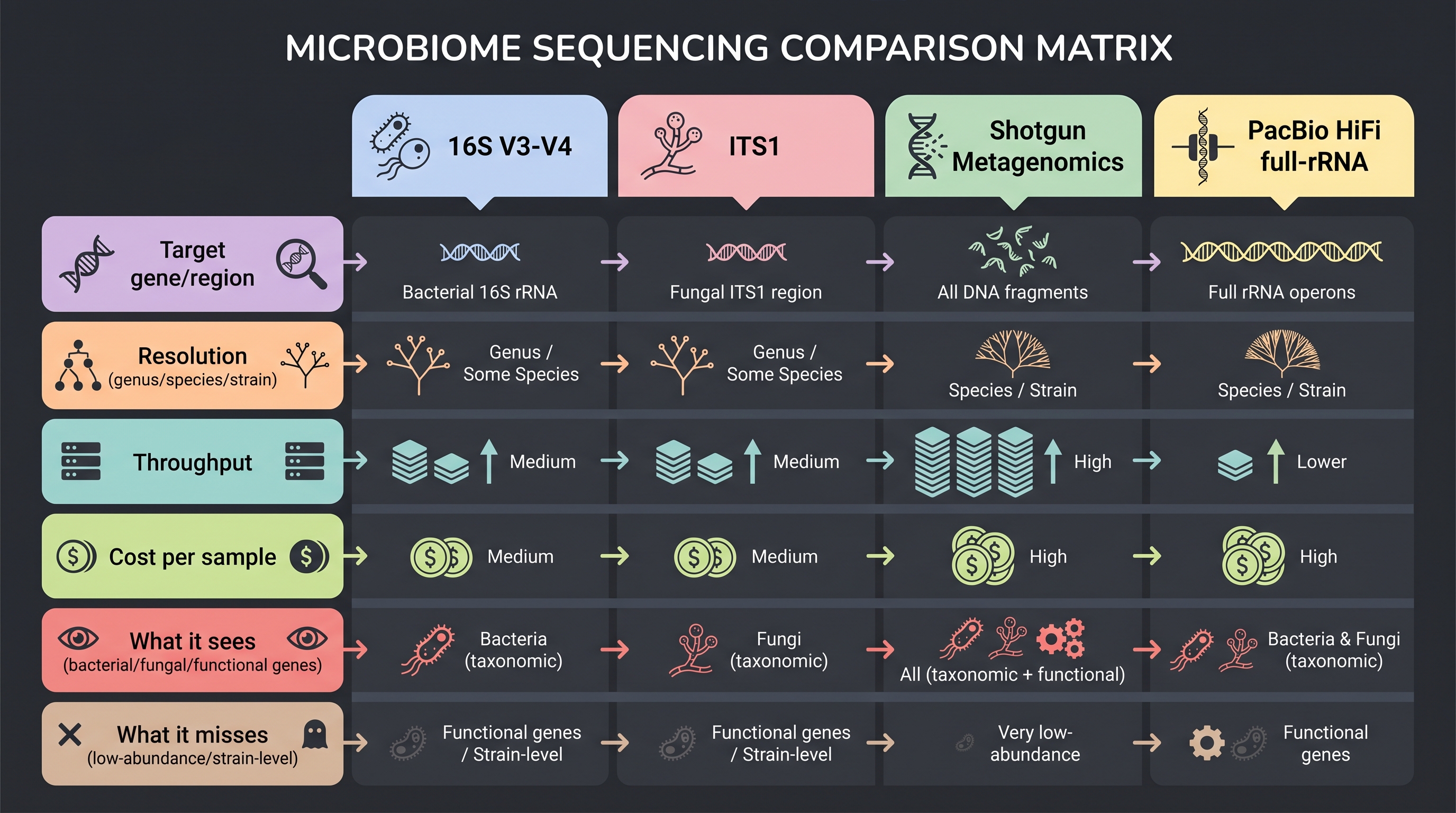
16S rRNA 유전자는 모든 세균이 가지고 있고(보존된 영역), 종 사이에 충분한 차이도 있어(가변 영역) 분류학에 이상적이다. V3–V4 영역을 primer로 증폭해 Illumina 짧은 read로 시퀀싱하는 방식이 사실상 표준이 되었다. 비용이 저렴해 코호트당 수백~수천 샘플도 다룰 수 있다.
[5]이 만든 QIIME은 OTU(Operational Taxonomic Unit, 97% 유사도) 기반 클러스터링을 표준화했다. 그러나 OTU 97%는 사실상 속(genus)에 가까운 종(species) 해상도다 — 같은 OTU 안에 효능이 다른 균주들이 섞여 들어가는 일이 흔했다. 이 한계를 깨뜨린 것이 [4] DADA2다. DADA2는 Illumina의 시퀀싱 오류를 통계적으로 모델링해 1-nucleotide 해상도의 ASV(Amplicon Sequence Variant) 를 추정한다. 이로써 OTU 97%로는 묶여 있던 균주 수준 다양성이 비로소 보이기 시작했다.
표준 reference 데이터베이스는 [17] SILVA, Greengenes, RDP 세 가지가 양분한다. Propionibacterium acnes가 Cutibacterium acnes로 재명명되는 등 분류 체계가 바뀔 때마다 reference DB의 업데이트 속도가 어긋나는데, 이는 학계·산업계 사이 데이터 호환성을 흔드는 작지만 끈질긴 문제다.
한계. 16S amplicon에는 세 가지 구조적 약점이 있다. (i) 증폭 영역(V1–V9 중 어느 부분을 쓰는지)에 따라 species-level 해상도가 다르다 — 예컨대 Staphylococcus는 V1–V3에서, Lactobacillus는 V3–V4에서 더 잘 구분된다. (ii) 곰팡이·바이러스는 안 보인다 — 곰팡이는 ITS, 바이러스는 별도 viromics가 필요하다. (iii) 가장 본질적으로, 16S는 누가 있는가만 알려주지 무엇을 하는가를 알려주지 못한다. 효능 가설을 세우기에는 부족하다.
3.3 ITS와 곰팡이 — Malassezia를 위한 별도의 망원경
피부 곰팡이는 16S 망원경에 잡히지 않는다. [6]은 ITS1 영역을 써서 처음으로 사람 피부 곰팡이 군집을 부위별로 매핑했다. 결과는 인상적이었다 — 몸통과 팔 11개 부위에서 Malassezia가 곰팡이 reads의 80% 이상을 차지하는 반면, 발은 Aspergillus·Cryptococcus·Rhodotorula까지 풍부한 별도의 생태계를 가졌다.
Malassezia는 화장품 영역에서 특히 중요하다. 비듬·지루성 피부염·아토피 피부염 일부 endpoint가 Malassezia 종 구성과 직접 연관되며 (Chapter 2), 따라서 항진균·항비듬 화장품의 효능 평가에 ITS 시퀀싱이 사실상 필수가 되었다. 단, ITS1은 단일 locus라 일부 Malassezia 종을 충분히 구분하지 못한다 — frontier에서는 ITS2 또는 long-read full-rRNA 접근이 보완책으로 쓰인다.
3.4 Shotgun metagenomics — 무엇을 하는가까지 보는 두 번째 망원경
Shotgun metagenomics는 미생물 군집의 전체 DNA를 무작위로 잘라 시퀀싱한다. amplicon이 분류학적 사진이라면 shotgun은 기능적 청사진에 가깝다. 단점은 명확하다 — 피부는 host(사람) DNA가 90% 이상을 차지하는 저 biomass 환경이라 충분한 미생물 read를 얻으려면 sample당 ~10 Gb 시퀀싱이 필요하고 비용도 16S의 10–50배다.
피부에서 shotgun metagenomics가 본격 가능해진 결정적 사건이 [14]다. NIH NHGRI Segre lab은 건강한 성인 15명의 18개 부위에서 270개 metagenome을 모아 세균·곰팡이·바이러스 모두를 다 본 첫 고해상도 카탈로그를 만들었다. 같은 그룹의 [15]은 후속 1–2년 시점에 같은 사람들을 다시 샘플링해 — 놀랍게도 — 피지가 많은 부위에서 균주 수준 안정성이 80% 이상이라는 사실을 보였다. 피부 마이크로바이옴은 우리가 생각한 것보다 훨씬 안정적이다. 이 결과는 "당신의 마이크로바이옴 균형을 잡아드립니다"라는 화장품 마케팅 카피의 과학적 토대인 동시에 그 한계 — 제품이 단기적으로 조성을 흔들기 어렵다는 — 의 출발점이기도 하다.
분석 도구도 같이 진화했다. [18] MetaPhlAn2는 clade-specific marker로 종 수준 식별을 빠르게 하고, 동봉된 StrainPhlAn 모듈은 균주 수준 추적까지 가능하게 한다. [1] HUMAnN은 reads로부터 KEGG/MetaCyc 대사 경로 abundance를 추정한다 — 효능 가설을 세우는 첫 번째 입력값이다.
iHSMGC와 데이터 비대칭. 그러나 reference 카탈로그가 어디서 만들어지느냐가 결과를 좌우한다. [11] iHSMGC는 한족(漢族) 822명의 shotgun 데이터에 기존 북미 538명 데이터를 통합해 총 10.9M개의 피부 유전자 카탈로그를 구축했는데, 이 중 4.88M개(약 45%)는 HMP를 비롯한 서구 reference에 없던 유전자였다. 같은 연구는 동아시아 얼굴 피부에 Moraxella osloensis-type과 Cutibacterium acnes-type이라는 두 가지 "cutotype"을 정의했다 — 북미 코호트에서는 M. osloensis가 거의 안 보였던 균이다.
iHSMGC가 던지는 메시지는 두 겹이다. 표면적으로는 "동아시아 소비자의 피부 마이크로바이옴은 서구 코호트로 추정하면 절반쯤 놓친다." 그 아래에는 더 무거운 신호가 있다 — 현재 공공 reference는 어디서 누가 만들었는지에 따라 체계적 사각지대가 생기며, AI 기반 효능 예측 모델이 train되는 데이터의 분포 역시 그만큼 편향된다. 이 문제는 (Chapter 4) AI 스크리닝, (Chapter 12) blueprint에서 다시 등장한다.
3.5 Long-read — 균주 해상도와 hybrid 조립
Illumina short-read shotgun은 150–300 bp 단위로 자른 조각을 다시 짜맞춘다. 반복 서열이 많거나 가까운 균주의 게놈을 구분해야 할 때 한계가 명확하다. PacBio HiFi(>15 kb, Q30+)와 Oxford Nanopore(수 kb–수 Mb) 같은 long-read 기술은 이 한계를 정면으로 푼다 — 한 read 안에 16S 풀 길이(약 1,500 bp)나 16S–23S 사이 ITS 영역까지 다 들어가 amplicon에서도 종·균주 해상도가 나오고, shotgun에서는 plasmid·repeat·mobile element가 보존된 채로 조립된다.
저비용 코호트는 여전히 Illumina + DADA2가 표준이지만, 균주 수준 정밀 분석이 필요한 화장품 R&D — 예컨대 (Chapter 7) 합성생물학 균주 엔지니어링이나 (Chapter 4) AI 균주 스크리닝의 ground truth — 에서는 long-read와 short-read를 함께 쓰는 hybrid가 사실상 표준이 되어 가고 있다. 가격이 떨어진 2024년 이후 일부 한국·중국 산업 코호트가 이를 본격 도입하기 시작했다.
3.6 Culturomics의 부활 — "배양은 죽었다"는 보고는 과장이었다
NGS가 등장한 직후 학계에는 "배양은 끝났다"는 분위기가 잠시 있었다. 그 분위기가 가장 강하게 뒤집힌 사건이 [10] Nature Reviews Microbiology의 culturomics 종합 리뷰다. Marseille IHU 그룹은 70종 이상의 배지, 다양한 가스 조성, MALDI-TOF MS 식별을 결합해 2018년까지 사람 미생물에서 1,000종 이상의 신규 배양 회수에 성공했다. 그중 다수는 그 직전까지 16S로만 알려져 있던 미배양 균이었다.
왜 배양이 돌아왔는가. 세 가지 이유가 겹친다.
첫째, 기능 검증. 16S/shotgun이 알려주는 것은 있다 또는 있을 가능성이 있다까지다. 항균·항염·항노화 같은 화장품 endpoint를 실측하려면 해당 균을 키워서 실제로 assay를 돌려야 한다. AI가 metabolite 후보를 추천해도 그 균을 손에 쥐고 발효시켜 추출해야 efficacy가 검증된다 (Chapter 4·5).
둘째, 균주 자원(strain bank). 합성생물학 시대의 R&D는 균주를 자산으로 본다 (Chapter 7). 시퀀스만으로는 균주를 보유하지 못한다 — 균주 카탈로그는 culture collection 형태로 존재해야 한다. ATCC, DSMZ, KCTC 같은 공공 culture bank에 더해, COSMAX·아모레퍼시픽·Galderma 같은 회사의 사내 culture collection은 핵심 IP다.
셋째, AI 예측의 ground truth. AI 모델이 "이 균주가 항염 효능이 있을 것"이라 예측해도 — 그 예측을 신뢰하려면 (a) 충분히 다양한 입력 분포에 대해 ground truth를 봐야 하고 (b) 새 예측이 들어왔을 때 검증 루프가 빠르게 돌아야 한다. 이 두 가지를 가능하게 하는 인프라가 high-throughput culturomics다. AI는 예측하고, 배양은 검증한다 — 이 한 줄이 책의 핵심 thesis다.
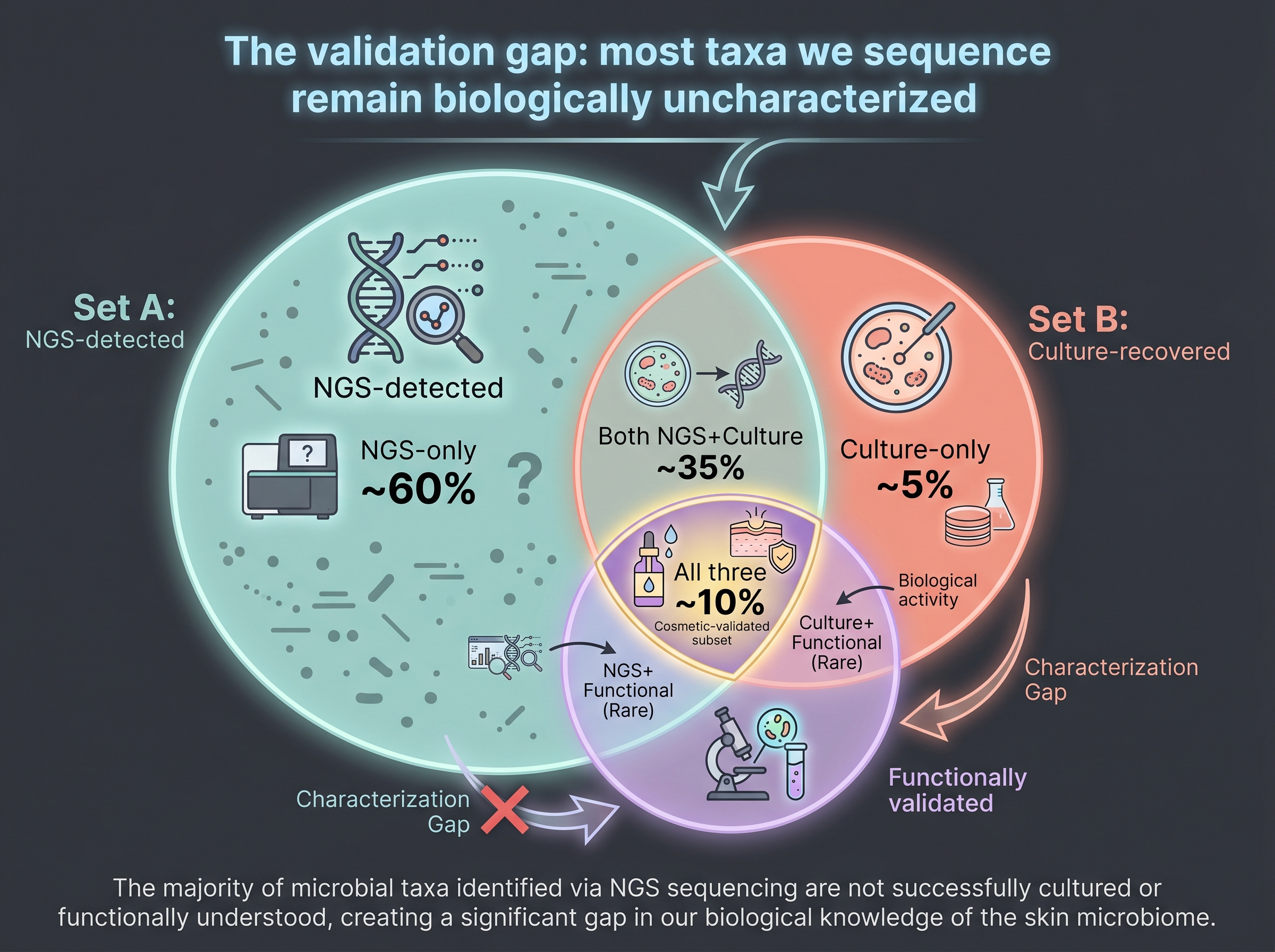
그러나 피부 culturomics는 여전히 약하다. Lagier 리뷰의 1,000+ 종 중 대부분은 장(gut) 유래다. 피부 culturomics는 (a) host DNA로 인한 식별 잡음, (b) 낮은 biomass, (c) 산소·CO₂·지질 의존 균의 까다로운 배지 요구 때문에 장 culturomics만큼 성숙하지 못했다. 코퍼스 단위로 보아도 피부 특이적 culturomics 논문은 [10] 외에는 frontier window에 거의 없다 — 이것이 책의 명시된 Gap 3이며 (Chapter 9) 임상 검증의 토대를 흔드는 약점이다.
가장 단단한 예외는 Gallo lab(UCSD)의 한 줄기 작업이다. [12]은 건강 피부 commensal Staphylococcus (특히 S. hominis, S. epidermidis)가 S. aureus를 죽이는 AMP(antimicrobial peptide)를 분비하며 이 항균 능력이 아토피 피부염 환자에서 부족하다는 것을 보였다. 이어 [13]은 S. hominis A9 균주를 분리·동정·배양·정량 후 54명 성인 아토피 환자에서 Phase 1 RCT를 진행해 7일 양일 도포로 S. aureus 부담을 70%의 환자에서 99% 감소시켰다. 매 단계가 wet-lab이고, AI는 거의 등장하지 않는다. 이 lineage가 보여주는 것은 — 기초 배양 연구가 단단할 때, AI 없이도 임상까지 갈 수 있다. AI는 이 lineage의 속도를 압축할 도구이지 대체재가 아니다.
3.7 그래서, 기초 연구는 구식이 되었는가 — Brief A에 대한 답
Brief A는 묻는다. "분리·동정·배양·기본 항균 항염 테스트 같은 기초 연구들은 이제 다 구식이 된 건가?"
이 책의 답은 아니오, 보완 관계다. 세 단계로 풀어 쓸 수 있다.
- AI는 검색·예측 비용을 압축한다. 수만~수십만 균주·대사체 후보에서 항균·항염·항노화 endpoint 후보를 좁히는 데 걸리는 시간이 wet-lab만 쓸 때와 비교해 한 자릿수 또는 두 자릿수 줄어들 수 있다 (Chapter 4·5).
- 배양·assay는 그 예측을 검증한다. 어떤 AI 모델도 실제 효능을 증명하지 못한다. AlphaFold가 예측한 단백질 상호작용은 docking score이지 in vitro efficacy가 아니다. (Chapter 5)에서 다시 다룬다.
- 검증된 균주·대사체는 다음 AI 라운드의 train data가 된다. 이 루프가 잘 도는 회사는 데이터 자산이 누적되고, 잘 안 도는 회사는 매번 처음부터 다시 한다. (Chapter 7) DBTL 루프의 원형이다.
따라서 "기초 연구가 구식인가"라는 질문은 잘못 던져진 질문이다. 옳은 질문은 — 우리 R&D 조직이 AI 예측 레이어와 배양·검증 레이어를 한 파이프라인으로 묶고 있는가, 아니면 둘이 사일로처럼 따로 있는가. 두 레이어가 묶여 있을 때만 (Chapter 9)의 임상 시뮬레이션, (Chapter 12)의 신규 연구 기획이 의미를 가진다.
[3]은 Nature Reviews Microbiology 리뷰에서 "피부 reference genome의 부족이 metagenomic 해상도를 여전히 제약한다"고 명시했다 — culturomics와 NGS의 동시 강화 없이는 그 제약이 풀리지 않는다. [8]가 만든 reference는 위대했지만 피부 sampling이 3곳뿐이었고, [11]이 보였듯 동아시아 코호트로 가면 또 다른 카탈로그가 나타난다. Reference의 빈틈을 메우는 일은 끝나지 않았다.
3.8 Open Questions — 재현성, 비용, 표준화
코퍼스 전반에서 미해결로 남아 있는 질문들. 이 챕터가 닫을 수 있는 것은 아니지만, 독자가 다음 챕터로 넘어가기 전에 머리에 두고 가야 할 것들이다.
- Kit·batch 효과를 어떻게 통제할 것인가. 동일 sample도 DNA 추출 kit이 다르면 alpha diversity가 통계적으로 유의하게 갈리는 경우가 흔하다 — [16]은 microbiome ML에서 batch effect를 consensus risk로 명시했지만 화장품 산업이 따르는 표준은 아직 형성되지 않았다. (gap.md Gap 8)
- Reference 카탈로그의 인종·지역 편향. iHSMGC는 한족, HMP는 북미 중심. 한국·일본·동남아·아프리카·라틴 아메리카 피부 reference는 코호트 단위로 거의 비어 있다. AI 효능 예측의 일반화는 그만큼 위태롭다.
- Cost vs depth의 trade-off. 코호트당 샘플 수를 늘릴 것인가, 샘플당 시퀀싱 깊이를 키울 것인가, 아니면 long-read로 가서 균주 해상도를 얻을 것인가. 가용 예산이 같다면 어느 조합이 화장품 endpoint 예측에 가장 도움이 되는가에 대한 합의된 답은 없다.
- 피부 culturomics를 어떻게 가속할 것인가. Marseille IHU의 장(gut) culturomics가 70+ 배지 + MALDI-TOF로 풀었다면, 피부 버전은 어떤 배지·기체 조성·식별 파이프라인이 필요한가. 이 질문에 대한 공개 합의는 없다 — 산업체 사내 collection은 누적되어 있지만 공유되지 않는다.
- Foundation model의 부재. ESM3·DNABERT 규모의 피부 마이크로바이옴 foundation model은 존재하지 않는다 ([9]; [7] ESM3 비교). 데이터가 사내에 잠겨 있는 한 (Chapter 12), 학계가 만들 길은 좁다.
이 다섯 질문은 다음 챕터들의 출발점이다. (Chapter 4)에서는 AI 균주·대사체 스크리닝이 어떻게 이 약점들을 부분적으로 회피하는지를, (Chapter 12)에서는 산업·학계가 함께 풀어야 할 인프라 청사진을 다룬다.
참고문헌
- Abubucker, S., Segata, N., Goll, J., et al. (2012). Metabolic reconstruction for metagenomic data and its application to the human microbiome. PLoS Computational Biology.
- Bolyen, E., Rideout, J. R., Dillon, M. R., et al. (2019). Reproducible, interactive, scalable and extensible microbiome data science using QIIME 2. Nature Biotechnology.
- Byrd, A. L., Belkaid, Y., & Segre, J. A. (2018). The human skin microbiome. Nature Reviews Microbiology.
- Callahan, B. J., McMurdie, P. J., Rosen, M. J., Han, A. W., Johnson, A. J. A., & Holmes, S. P. (2016). DADA2: High-resolution sample inference from Illumina amplicon data. Nature Methods.
- Caporaso, J. G., Kuczynski, J., Stombaugh, J., et al. (2010). QIIME allows analysis of high-throughput community sequencing data. Nature Methods.
- Findley, K., Oh, J., Yang, J., et al. (2013). Topographic diversity of fungal and bacterial communities in human skin. Nature.
- Hayes, T., et al. (2025). Simulating 500 million years of evolution with a language model (ESM3). Science. [Hayes et al., 2025]
- Human Microbiome Project Consortium (2012). Structure, function and diversity of the healthy human microbiome. Nature. [HMP Consortium, 2012]
- Wang, X.-W., Wang, T., & Liu, Y.-Y. (2024). Artificial Intelligence for Microbiology and Microbiome Research. arXiv. [Wang et al., 2024]
- Lagier, J.-C., Edouard, S., Pagnier, I., Mediannikov, O., Drancourt, M., & Raoult, D. (2018). Culturing the human microbiota and culturomics. Nature Reviews Microbiology.
- Li, Z., Xia, J., Jiang, L., et al. (2021). Characterization of the human skin resistome and identification of two microbiota cutotypes (iHSMGC). Microbiome.
- Nakatsuji, T., Chen, T. H., Narala, S., et al. (2017). Antimicrobials from human skin commensal bacteria protect against Staphylococcus aureus and are deficient in atopic dermatitis. Science Translational Medicine.
- Nakatsuji, T., Hata, T. R., Tong, Y., et al. (2021). Development of a human skin commensal microbe for bacteriotherapy of atopic dermatitis and use in a phase 1 randomized clinical trial. Nature Medicine.
- Oh, J., Byrd, A. L., Deming, C., Conlan, S., NISC Comparative Sequencing Program, Kong, H. H., & Segre, J. A. (2014). Biogeography and individuality shape function in the human skin metagenome. Nature.
- Oh, J., Byrd, A. L., Park, M., NISC Comparative Sequencing Program, Kong, H. H., & Segre, J. A. (2016). Temporal Stability of the Human Skin Microbiome30399-3). Cell.
- Papoutsoglou, G., et al. (2023). Machine learning approaches in microbiome research: challenges and best practices. Frontiers in Microbiology. [Papoutsoglou et al., 2023]
- Quast, C., Pruesse, E., Yilmaz, P., Gerken, J., Schweer, T., Yarza, P., Peplies, J., & Glöckner, F. O. (2013). The SILVA ribosomal RNA gene database project: improved data processing and web-based tools. Nucleic Acids Research.
- Truong, D. T., Franzosa, E. A., Tickle, T. L., Scholz, M., Weingart, G., Pasolli, E., Tett, A., Huttenhower, C., & Segata, N. (2015). MetaPhlAn2 for enhanced metagenomic taxonomic profiling. Nature Methods.