Chapter 4: AI 기반 균주·메타볼라이트 스크리닝
왜 이 챕터인가
Part I이 "무엇이 바뀌었는가"를 보여주었다면, Part II는 "왜 AI가 변곡점이었는가"를 답해야 한다. 그 첫 번째 답은 스크리닝(screening)에서 나온다. 마이크로바이옴 화장품 R&D가 다뤄야 할 후보의 규모는 인간이 손으로 검증할 수 있는 한계를 이미 넘어선 지 오래다 — 피부 마이크로바이옴 단일 사이트만 봐도 수백 종(species)·수천 균주(strain), 각 균주는 수십~수백 개의 생합성 유전자 클러스터(biosynthetic gene cluster, BGC)를 갖고, 각 BGC가 잠재적으로 새 대사체 한 분자 이상을 코딩한다. 화장품 endpoint(항균·항염·항산화·항노화)마다 wet-lab 표준 assay 한 번에 수십~수백 달러가 든다. 모든 후보를 전부 직접 시험하는 것은 산술적으로 불가능하다.
머신러닝의 역할은 단순하다: wet-lab 검증을 받기 전에 후보의 우선순위를 매기는 것. 약학 산업은 이 일을 30년 이상 해왔다 — Tanimoto 유사도 기반 hit triage부터 시작해 [25]이 발견한 halicin, [29]의 GENTRL DDR1 억제제, [22]의 rentosertib(임상 2a)까지. 화장품·마이크로바이옴은 같은 도구를 5~10년 늦게 도입하는 중이지만, 도메인 데이터의 형태가 다르기 때문에 단순한 이식은 통하지 않는다. 이 챕터는 그 차이를 정리한다.
이 챕터의 정량적 핵심 3가지 1. 효능 endpoint별 ML 파이프라인의 형태: 분자 fingerprint → classical ML → graph/transformer 모델의 진화. [25]의 MPNN, [3]의 SHAP 기반 XAI가 분기점. 2. 데이터 소스의 구조: 메타볼라이트 쪽은 공개(NPAtlas·MIBiG·GNPS)가 작동, 균주·임상 endpoint 쪽은 사실상 비공개(Unilever 30K, COSMAX FACE-LINK 950명). 이 비대칭이 모델 일반화의 천장을 결정한다. 3. 산업 사례 5건: Insilico (제약), Cradle·Profluent (단백질 SaaS), COSMAX × Dankook FACE-LINK (한국 화장품), L'Oréal × Lactobio (M&A 통한 데이터 확보), Unilever (XAI 사내 파이프라인). 화장품 산업은 아직 AI로 설계된 활성 성분의 동료 심사 임상 결과를 발표한 적이 없다 — Gap 1.
4.1 스크리닝 병목 — AI 이전의 수치
발효 화장품 시대(Chapter 1)의 활성 성분 발견은 본질적으로 경험·우연·역설계의 조합이었다. SK-II의 Pitera는 사케 양조장 노동자의 손에서 시작했고, Galactomyces ferment filtrate의 AHR 작용 기전은 [26]가 분리해낸 2015년에야 분자 수준에서 풀렸다 — 제품이 시장에 나온 지 30년 후의 일이다. 메타지노믹스 시대(Chapter 3)가 열리자 후보 공간이 폭증했다. 단일 피부 메타지노믹 catalog인 iHSMGC만 해도 1,094만 개 유전자를 등록했고, 그 중 ~45%는 기존 HMP에 보이지 않던 신규였다 [16].
이 규모를 가장 직관적으로 보여주는 수는 BGC 카운트다. [2]는 피부·구강·장 마이크로바이옴 전체에서 antiSMASH로 식별된 BGC가 인당 평균 수백 개, 종 단위로 보면 모르는 RiPP(ribosomally synthesized post-translationally modified peptide)·NRPS(non-ribosomal peptide synthetase)·PKS(polyketide synthase) 클러스터가 더 많다는 점을 강조한다. 한 클러스터의 산물을 실제로 분리·구조 결정·assay까지 가져가려면 보통 박사 연구원 한 명이 6~24개월을 쓴다. 모든 BGC를 균등하게 추적하는 것은 인력 산술상 불가능하다.
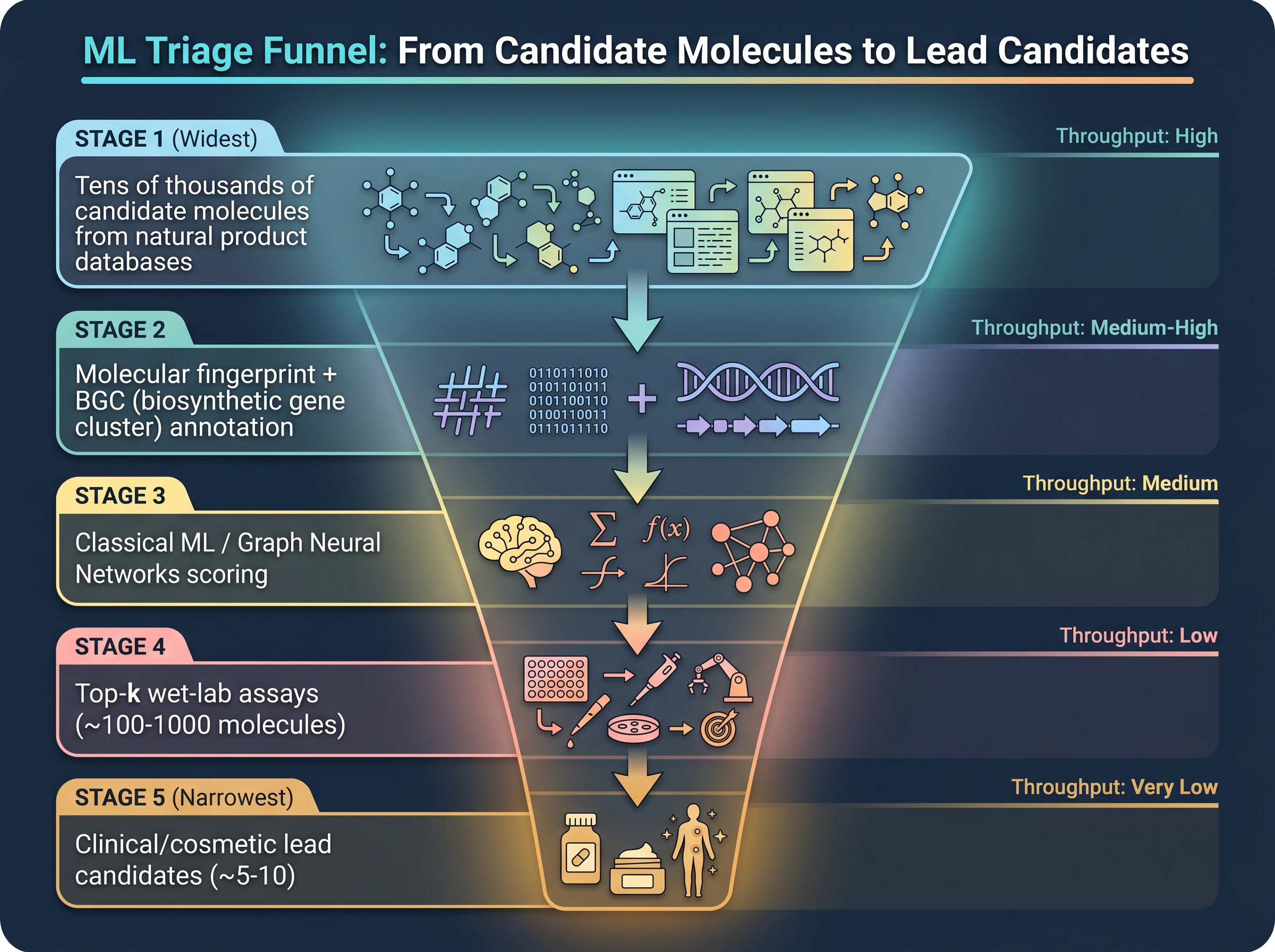
그렇다고 무작위로 추리면 hit rate가 떨어진다. [25]의 halicin 연구는 이 비대칭을 정확히 활용했다 — 2,335개 분자의 primary library로 message-passing neural network(MPNN)을 학습시킨 뒤, 6,111개로 큐레이트된 Drug Repurposing Hub(FDA 승인·임상 시험 단계 약물 모음)에 모델 점수를 매겼다. 모델 상위 99개 후보를 E. coli 대장균에 wet-lab 검증한 결과 51개(51.5%)가 활성을 보였고, 그 51개를 다시 화학 구조 다양성·toxicity·발견된 항생제와의 유사성으로 필터링해 1~3개가 남았다 — 가장 유명한 후보가 halicin이다. 이 수치는 항생제(가장 잘 정의된 endpoint)의 경우다. 화장품 endpoint — "항노화 효능", "민감성 피부 진정" — 는 단일 in vitro assay로 환원하기 더 어렵기 때문에 baseline hit rate가 더 낮을 가능성이 높다. 정확한 수치는 산업 내부 데이터에 갇혀 있다 [8].
ML triage의 약속은 잡음 라이브러리의 1% 미만 hit rate를 모델 상위 후보 풀에서 30~50%대로 끌어올리는 것이다 — halicin 연구가 보여준 51.5%(상위 99개 중 51개)는 랜덤 추출의 수십 배에 해당하는 비율이며, wet-lab 처리량이 ML triage의 출력을 산업적으로 의미 있게 받아낼 수 있는 수준이다. 화장품에서 동급 외부 검증을 발표한 연구는 — Gap 1에서 후술하듯 — 아직 없다.
4.2 효능 endpoint 카탈로그 — 같은 도구, 다른 proxy
화장품 ML이 약학 ML과 다른 가장 큰 이유는 endpoint의 정의 자체가 약하다는 점이다. 항생제는 MIC(minimum inhibitory concentration)라는 단일 in vitro 측정으로 환원되지만, "항노화"는 그렇지 않다. 어느 정도의 단순화·환원이 가능한 endpoint와 그렇지 않은 endpoint가 분리되며, 그것이 모델의 가용 데이터 규모를 결정한다.
항균(antimicrobial) — 가장 잘 정의된 endpoint다. E. coli·S. aureus·C. acnes 등 표적 균에 대한 MIC, MBC(minimum bactericidal concentration)가 공통 화폐. [25]의 MPNN이 그대로 적용되며, [15]는 commensal Staphylococcus epidermidis가 epifadin이라는 폴리엔 펩타이드를 만들어 비강 S. aureus를 제거하는 사례를 보고했다 — 화장품 industries에 이미 정착한 "균이 균을 잡는다(microbe vs microbe)" 컨셉의 분자 기전. [24]은 그 흐름의 화장품 확장으로, AI로 피부 마이크로바이옴의 biotic·xenobiotic 대사를 예측하는 첫 도구다.
항염(anti-inflammatory) — proxy assay 분기가 시작된다. NF-κB·AP-1 reporter cell assay, IL-6·IL-8·TNF-α 분비 억제, AHR/NRF2 활성화. [9]가 NRF2 축으로 Galactomyces ferment filtrate의 두 번째 분자 기둥을 보완했지만, 모델의 입력은 일반적으로 분자 fingerprint나 펩타이드 서열, 출력은 다중 reporter assay의 정량 점수가 되며 그 매핑이 endpoint마다 다르다. 단일 모델이 여러 endpoint를 동시에 예측하는 multi-task learning이 자연스러운 형태가 되는 이유다.
항산화(antioxidant) — DPPH, ABTS, ORAC, 그리고 cell-based ROS 측정. 분자 fingerprint에서 ORAC 점수를 예측하는 QSAR 모델은 이미 1990년대에 안정화됐고, deep learning은 정확도를 점진적으로 끌어올렸다. 화장품 도메인에서 이는 가장 commoditized된 endpoint다.
항노화(anti-aging) — 본질적으로 합성 endpoint. 콜라겐 합성(procollagen ELISA), MMP-1 발현 억제, fibroblast senescence marker(SA-β-gal, p16), 종합 점수로 dermal density·wrinkle depth의 in vivo 측정. 단일 in silico endpoint로 환원할 수 없어, multi-omics 통합(transcriptomics + metabolomics + 임상 영상)이 학습 신호의 핵심이다. [28]의 skin microbiome aging 종설은 이 endpoint의 인과적 미해결성을 명시한다 — 상관은 풍부하지만 인과 사슬은 일부만 풀려 있다.
표 4.1 — endpoint별 ML 입력·출력·일반화 천장 | endpoint | 모델 입력 | 표적 출력 | 공개 데이터 규모 | 일반화 천장 | |---|---|---|---|---| | 항균 (MIC) | 분자 graph, 펩타이드 서열 | MIC ≤ 임계값 (이진) | ChEMBL, PubChem, MIBiG | 우수 — 외부 검증 가능 | | 항염 (NF-κB) | 분자 fingerprint | reporter 억제율 (회귀) | 중규모, 일부 공개 | 중간 — assay 변동성 | | 항산화 (ORAC) | 분자 fingerprint | ORAC 단위 (회귀) | 중규모, 다수 공개 | 우수 — 가장 commoditized | | 항노화 (collagen) | 분자 + multi-omics | procollagen + MMP-1 + 임상 영상 | 사실상 비공개 | 낮음 — 사내 데이터 의존 |
이 표가 곧 Gap 2(피부 마이크로바이옴 foundation model이 없다)와 Gap 12(공개 벤치마크가 없다)가 발생하는 지점이다 — 항노화·항염 같은 화장품 핵심 endpoint일수록 데이터가 사적이고, 그 결과 모델은 산업 내부에서 검증·재학습되며 외부 비교 가능성이 사라진다 [20].
4.3 데이터 소스 — 메타볼라이트는 공개, 균주는 비공개
화장품·마이크로바이옴 ML의 데이터 지형은 두 갈래로 갈라진다.
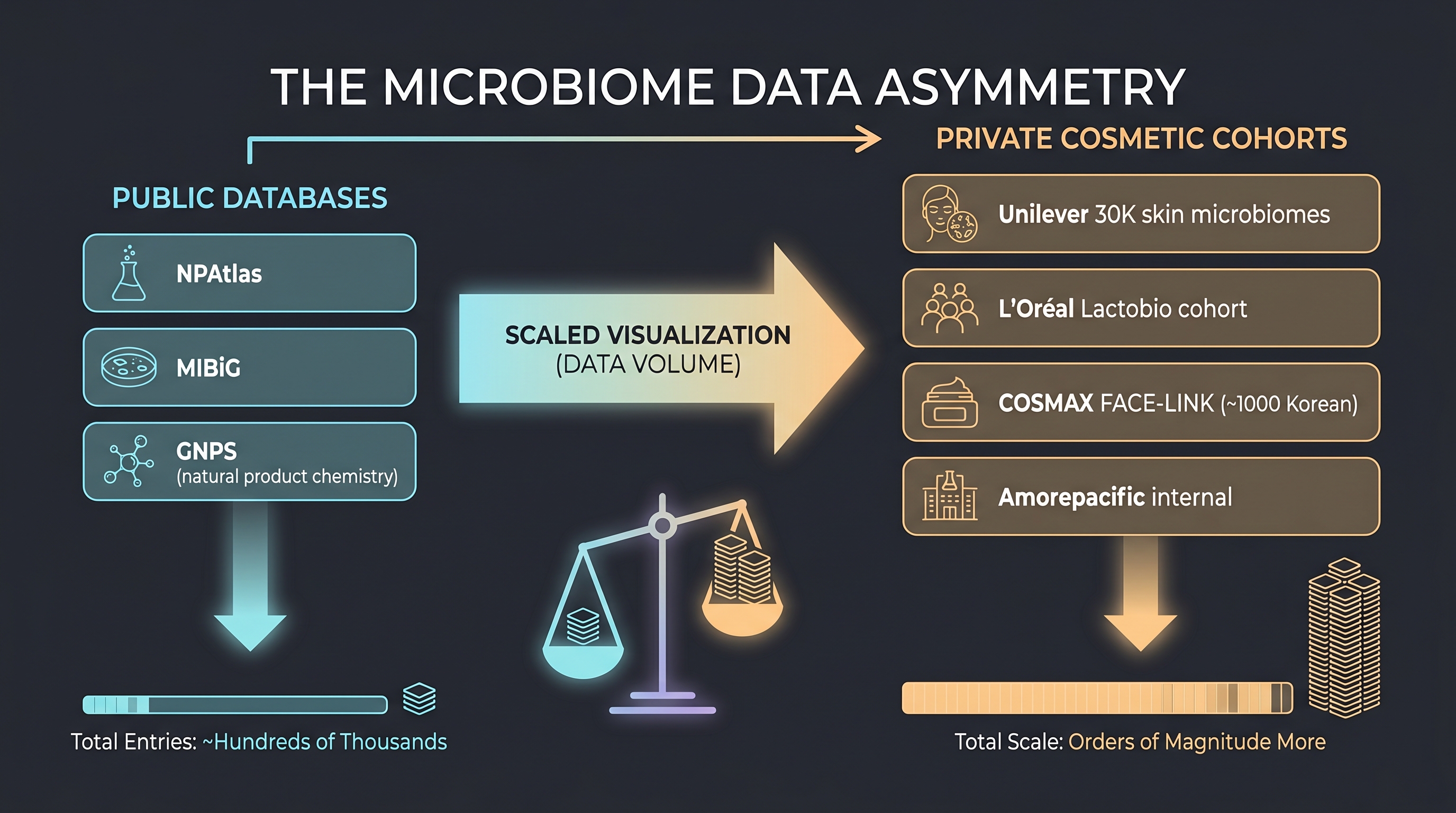
메타볼라이트(공개 자산)
- NPAtlas — 미생물·해양 천연물 분자의 공개 카탈로그. 2025년 현재 수만 분자가 SMILES·MOL·구조 분류와 함께 색인되어 있어 화장품 ML 모델의 분자 fingerprint 학습에 가장 자주 쓰이는 출발점이다.
- MIBiG (Minimum Information about a Biosynthetic Gene cluster) — BGC와 산물의 큐레이트 링크. antiSMASH 어노테이션에서 시작해 산물 분자까지 추적할 수 있는 ground-truth 셋트로, [2]가 강조하듯 화장품용 신규 RiPP·NRPS 탐색의 출발 인프라.
- GNPS (Global Natural Products Social) — MS/MS 스펙트럼 공개 저장소. 화장품 회사가 자체 metabolomics 데이터를 NPAtlas·MIBiG와 매핑할 때 표준 spectrum library.
- FAST-NPS — [7]가 Cell Systems에 발표한 고처리 자동화 genome mining 파이프라인. Streptomyces 등에서 BGC → 산물 → MS-guided 정제를 한 트랙으로 잇는 형태로, 화장품용 균주(S. epidermidis, C. acnes, Cutibacterium)로의 이식이 다음 단계 과제.
이 메타볼라이트 인프라는 학술-산업 협업의 결과로 비교적 공개적이며, 분자 fingerprint 기반 ML 모델(MPNN, Graph Transformer)이 곧장 학습할 수 있다.
균주·임상 endpoint(비공개 자산)
- HMP / iHSMGC / MGnify — 분류 정보와 유전자 카탈로그는 공개되어 있지만, 화장품 endpoint(피부 영상, 임상 점수)와 매핑된 메타데이터는 보통 부재.
- Unilever 사내 데이터 — [27]가 공개한 자체 추산으로 30,000 샘플, 50억 데이터 포인트. 외부 접근 불가.
- L'Oréal 사내 데이터 — Modjoul, Modiface 디바이스 데이터에 더해 Lactobio 인수([17])로 약 10,000균주 분리 collection을 흡수.
- COSMAX × Dankook FACE-LINK — 950명 한국인 cohort로 피부 마이크로바이옴 ↔ biophysical 측정 매핑 [18]. Chapter 10에서 자세히 다룰 한국형 사내 데이터의 대표 사례. (주: "FACE-LINK"는 COSMAX의 사내 플랫폼·제품 브랜드명이며, [18] 논문 본문은 이 명칭을 직접 사용하지 않는다 — 본 책에서는 COSMAX 측 공개 자료에 따라 두 호칭을 같은 코호트의 학술/상업 양 측면으로 표기한다.)
- EPI-7 임상 — [13]가 Epidermidibacterium keratini EPI-7 유래 postbiotics의 8주 RCT 효능을 보고한 한국 자료. 균주-임상 endpoint 매핑이 동료 심사 채널로 나온 드문 사례.
비대칭은 명백하다 — 메타볼라이트 쪽에서는 학술적 ML 진보가 가능하지만, "어떤 균주가 어떤 사람의 어떤 피부 endpoint를 개선하는가"는 회사 내부 데이터 없이 학습할 수 없다. [20]의 ML for microbiome 가이드라인이 강조하는 batch effect, compositionality, kit bias는 이 비대칭 위에서 두 배로 어렵다. [14]가 종합한 AI-microbiome 200+ 논문 중 피부 endpoint와 직접 매핑된 외부 검증 가능 모델은 매우 드물다.
4.4 Classical ML 베이스라인 — 사라지지 않은 30년 도구
AI hype의 그늘에 가려져 있지만, 현재 화장품·마이크로바이옴 ML의 실무 베이스라인은 여전히 random forest와 gradient boosting이다. 이유는 단순하다 — endpoint별 학습 데이터가 수백~수천 샘플 수준이고, 그 규모에서는 deep learning이 trivial하게 이기지 못한다. [3]의 IBM × Unilever 협업은 그 대표 사례다. 약 50명 코호트 16S 데이터에서 phenotype(피부 상태) 차이와 연관된 균종을 예측할 때, 그들은 gradient boosting + SHAP(Shapley value 기반 explainability)을 썼다. CNN이나 Transformer를 끼워 넣지 않은 이유는 이론적 우아함이 아니라 데이터 규모 — 50명 cohort에서 deep model을 학습시키면 overfit이 보장된다.
Tanimoto 유사도 기반 hit prioritization은 마찬가지로 화학정보학의 표준이다. 분자 fingerprint(Morgan, MACCS, RDKit)를 비트 벡터로 표현한 뒤, 알려진 활성 화합물(예: 알려진 항노화 펩타이드)과의 Tanimoto 거리 < 0.3을 만족하는 후보를 추리는 것은 — 화려하지 않지만 — wet-lab 우선순위를 가장 빠르게 좁히는 방법이다.
화장품 산업에서 classical ML이 여전히 우세한 또 하나의 이유: 해석 가능성. 마케팅 클레임을 뒷받침할 때 "deep learning이 그렇게 예측했다"는 진술은 규제·법무 검토를 통과하기 어렵다. SHAP·LIME·feature importance가 산출하는 변수 중요도는 R&D 회의에서 의사결정으로 옮길 수 있는 단위이고, 화장품 산업은 이 점에서 약학보다 더 보수적이다 [6].
4.5 Sequence-to-function 신경망 — AlphaFold 이전과 이후의 가교
엔드포인트 예측을 분자 fingerprint에서 출발하는 것은 이미 분리된 분자가 있을 때 통한다. 그러나 마이크로바이옴 ML의 진짜 야망은 메타지노믹 read에서 곧장 효능 후보 분자까지 가는 것이다. 그 흐름의 핵심 알고리즘들이 2020년대 초·중반에 자리잡았다.
DeepBGC, antiSMASH + ML — 메타지노믹 read나 조립된 contig에서 BGC 영역을 검출하는 모델. antiSMASH는 규칙 기반(hidden Markov model)이 출발점이었고, DeepBGC는 word2vec 임베딩 + Bidirectional LSTM으로 정확도를 끌어올린 2019년 시도. 출력은 "이 contig에 BGC가 있다, 산물은 X 클래스(RiPP/NRPS/PKS/terpene…)일 가능성이 높다"이며, 화장품 R&D에서 균주 collection을 BGC density로 정렬하는 데 직접 쓰인다. [7]는 이 흐름의 산업화 단계다 — Streptomyces genome → BGC → 산물 후보까지 한 파이프라인.
RFM(Retrosynthesis & Function Mining) — 메타지노믹 → 펩타이드 → 효능. 항균 펩타이드(AMP)의 경우 이 흐름이 가장 성숙해 있다. ESM-2 같은 단백질 언어 모델로 펩타이드 서열을 임베딩한 뒤, 항균 활성 분류기를 fine-tune하는 형태. 화장품 산업에서 S. epidermidis commensal이 생산하는 lugdunin류·epifadin류 펩타이드[15]를 비슷한 메타지노믹 균주에서 더 찾아내는 것이 가까운 산업 과제다.
Graph neural network for community function — 단일 균이 아닌 균 군집 수준에서 기능을 예측하는 흐름. 종간 상호작용을 그래프로 표현하고 message passing으로 community-level metabolite 생산을 예측한다. Chapter 6에서 디지털 트윈 맥락으로 더 다룰 이 흐름은, [14]와 [5]가 동시에 강조하는 현재 가장 활발한 학술 영역이지만, 임상 endpoint와 매핑된 검증 사례는 여전히 드물다.
이 모든 흐름에 공통된 한계: 검증의 ground truth는 결국 wet-lab. ML이 BGC 클래스를 예측해도 산물 분자의 정확한 구조는 NMR/MS로 결정해야 하고, 펩타이드의 항균 활성은 결국 plate assay로 확인해야 한다. 이 점이 Chapter 3의 메시지와 정확히 맞물린다 — 기초 연구는 구식이 아니다. AI가 가속하지만, 검증은 손이 한다.
4.6 산업 사례 — 5개 모델, 5개 메시지
4.6.1 Insilico Medicine — 화장품이 가진 적 없는 임상 readout
Insilico Medicine은 화장품 회사가 아니지만, AI로 설계된 활성 성분의 임상 readout 발표 가능성을 보여준 유일한 회사다. 2019년 GENTRL [29]은 강화학습 기반 generative model로 DDR1 kinase 억제제 후보를 ~46일 만에 합성·in vitro 검증까지 갔다 — 그 자체는 단발성 paper지만, 발견 비용 곡선의 새 기울기를 보여준 사건이었다. 같은 그룹이 발전시킨 PandaOmics 플랫폼 [21]은 target identification에서 약물 후보 추출까지 한 워크플로우로 통합한다.
가장 결정적인 readout은 2024년의 rentosertib(ISM001-055)다. [22]가 Nature Biotechnology에 보고한 end-to-end generative AI 발견 — target identification(PandaOmics) → 분자 설계(GENTRL/Chemistry42) → Phase 1까지 30개월. 이어 2025년 [12]는 Nature Medicine에 phase 2a 결과를 발표 — TNIK 억제제로 idiopathic pulmonary fibrosis 환자의 FVC(forced vital capacity)가 12주 후 위약 대비 +98.4 mL vs −20.3 mL로 우월. 이것은 AI 약물 발견 분야가 동료 심사 임상 readout을 가진 첫 사례 중 하나이며, 화장품 산업이 가진 적 없는 readout이다.
화장품으로의 시사: 화장품 endpoint(항노화, 진정)에서 동일한 워크플로우(target → 분자 설계 → 임상)를 실행하려면 — endpoint 정의를 충분히 좁히고, 임상 단계까지 가져갈 자본·시간 의지가 필요하다. Chapter 9·12에서 이 템플릿이 화장품에 어떻게 이식 가능한지, 그리고 왜 아직 아무도 시도하지 않았는지를 본격 분석한다.
4.6.2 Cradle Bio, Profluent — 단백질 설계의 SaaS 화
화장품 활성 성분 중 단백질·펩타이드는 새 시대의 핵심 후보다. 비건 콜라겐, 활성 펩타이드, 효소형 active 모두 단백질 설계 문제로 환원된다. Cradle Bio(취리히/델프트)는 generative 단백질 설계를 SaaS 형태로 제공하는 회사로 2024년 11월 $73M Series B를 마감했고 [4], 같은 시기 [19]가 Cradle을 고객으로 공개 — pharma 메이저가 in-house 모델을 모두 만들지 않고 외부 플랫폼을 쓰는 패턴의 첫 검증.
Profluent는 [23]가 bioRxiv에 발표한 ProGen2 기반 OpenCRISPR-1로 더 화제가 됐다 — CRISPR-Cas 단백질 우주를 학습한 언어 모델로 새 게놈 편집기를 생성, 그 일부를 오픈소스로 공개. Cradle은 closed-SaaS, Profluent는 open + commercial — 두 비즈니스 모델이 단백질 설계 시장에서 동시에 살아남고 있다.
화장품 시사: 화장품 회사가 단백질 설계 인프라를 자체 구축하지 않아도 된다는 메시지가 가장 중요하다. 비건 콜라겐, 펩타이드 active를 외부 SaaS에 발주하는 형태가 시간 단축에 직결되며, 산업 변동 속도가 화장품 출시 사이클(보통 18~24개월)에 맞을 만큼 빨라졌다. Chapter 7에서 합성생물학 DBTL 루프와 함께 더 다룬다.
4.6.3 COSMAX × Dankook FACE-LINK — 한국형 사내 데이터의 첫 공개 readout
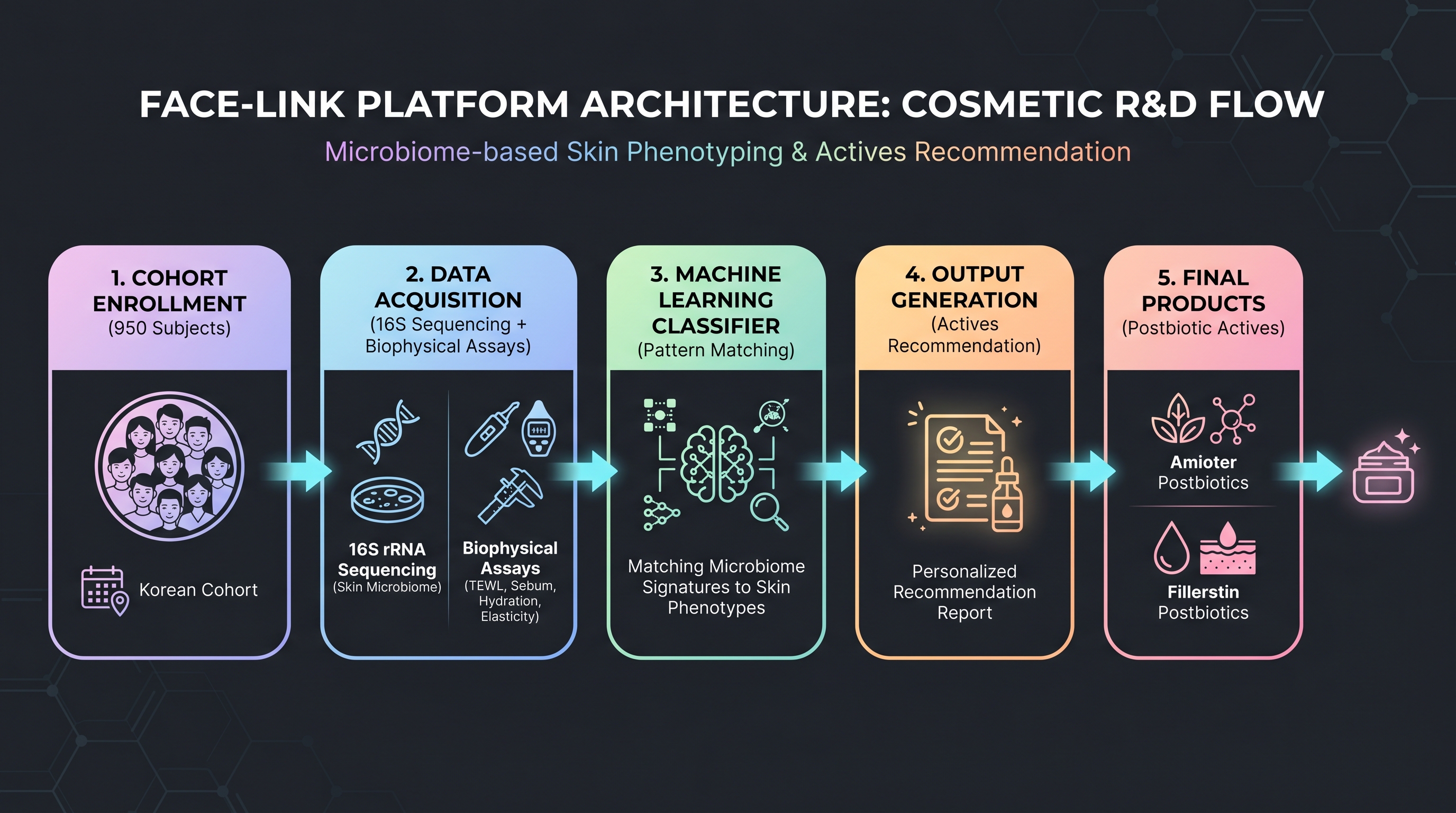
[18]는 Frontiers in Cellular and Infection Microbiology에 950명 한국인 코호트의 피부 마이크로바이옴-biophysical 측정 통합 분석을 발표했다 — FACE-LINK 플랫폼의 첫 동료 심사 readout. 16S 데이터에 더해 피부 수분, TEWL(transepidermal water loss), 멜라닌·홍반 측정이 같은 개인에서 매칭되어 있고, 한국인 피부 타입과 노화 그룹을 마이크로바이옴 시그니처로 분류하는 ML 모델이 검증됐다.
이 사례가 중요한 이유는 데이터 규모가 아니라 데이터 구조다 — Western 학술 cohort 대다수가 16S만 갖거나 metabolomics만 가지는 반면, FACE-LINK는 마이크로바이옴 + biophysical을 한 개인 단위로 매칭한다. 이런 매칭 cohort는 ML의 supervised learning 기반이 되며, 그 결과 화장품 endpoint와 직접 매핑된 모델을 학습할 수 있다.
한국 산업의 구조적 자산: COSMAX는 B2B OEM이라 발표가 비즈니스에 도움이 된다 — 동종 OEM이 없는 Western 화장품 산업과 다른 점이다. Amorepacific·LG생활건강은 B2C 브랜드라 발표 인센티브가 약하다(Gap 4). FACE-LINK는 그 결과 한국에서 거의 유일하게 외부 가시성을 가진 사내 cohort다. Chapter 10에서 한국 산업 매트릭스 안에서 더 분석한다.
4.6.4 L'Oréal × Lactobio — M&A로 데이터를 사다
L'Oréal은 2023년 12월 덴마크 마이크로바이옴 회사 Lactobio를 인수했다 [17] — 거래는 2024년 1분기에 완료. Lactobio가 가져온 자산은 두 가지: (1) 분리·동정된 ~10,000 균주의 사내 culture collection, (2) 그 균주의 효능 데이터(주로 항균·항염 in vitro). L'Oréal R&D는 기존의 분자·peptide AI 파이프라인에 균주 자산을 결합해 — Chapter 10에서 다룰 Modjoul/Modiface 디바이스 데이터와 함께 — multi-modal 화장품 마이크로바이옴 R&D 인프라를 구축 중이다.
전략 메시지: 화장품 산업에서 AI를 키우는 것보다 데이터를 사는 게 더 빠른 길이라는 인식. ML 모델 아키텍처는 academic AI가 빠르게 commodity로 만들지만, 균주 collection과 임상 endpoint 매핑 데이터는 commodity가 아니다. L'Oréal Lactobio 인수는 그 비대칭에 대한 합리적 반응이며, 이후 산업 M&A 패턴의 템플릿이 됐다.
4.6.5 Unilever — XAI 사내 파이프라인의 표준화
[3]은 Unilever R&D와 IBM Research가 공동 저자로 발표한 Scientific Reports 논문으로, gradient boosting + SHAP을 써서 피부 마이크로바이옴 composition에서 phenotype(피부 상태) 차이를 예측한 사례를 보고했다. 이 논문은 화장품 산업이 발표한 방법론적으로 책임 있는 ML 적용의 첫 사례 중 하나이며 — n=1 academic publication이지만 — Unilever 사내 파이프라인의 표준화 출발점으로 해석된다.
2025년 [27]가 SXSW와 자체 R&D 페이지에서 공개한 수치는 다음과 같다 — 30,000 샘플, 50억 데이터 포인트의 사내 cohort, AI virtual cohorts(2,500명 시뮬레이션 코호트), formulation cycle을 5~6에서 1~2로 단축, claims development 75% 가속. operational KPIs는 인상적이지만 외부 검증은 없다(Gap 15). [10]의 PRISMA 종설은 cosmetogenomics 분야의 AI 적용 74편을 정리하면서, L'Oréal·Unilever를 포함한 어떤 회사도 — 외부 동료 심사된 — AI 디자인 활성 성분의 임상 readout을 발표한 적이 없다고 명시한다.
이 두 사례(Carrieri 2021의 외부 가시성 vs Unilever 2025의 내부 KPI)의 간극이 곧 Gap 1 — 화장품 산업에서 AI는 발견·triage·formulation에 적극 쓰이고 있지만, 임상 단계까지 가져간 readout이 아직 동료 심사 채널로 나오지 않았다.
4.7 The Gap — Insilico의 readout이 화장품에 없다 (Chapter 9·12와의 연결)
이 챕터의 가장 중요한 한 줄: 2026년 5월 현재, AI로 설계된 화장품 활성 성분의 동료 심사된 임상 시험 결과는 존재하지 않는다. 도구는 준비되어 있다 — AlphaFold 3 [1], ESM3 [11], generative 분자 디자인, BGC mining 모두 2024년 기준 commodity. 데이터도 사적이지만 충분히 존재한다 — Unilever 30K, COSMAX FACE-LINK 950, L'Oréal Lactobio 10K 균주. 산업 인센티브만 부족하다.
[10]가 명시하는 이유는 두 가지다. (1) 화장품 활성 성분은 약물처럼 FDA 승인을 받지 않아도 되기 때문에 동료 심사 임상 readout의 상업적 ROI가 낮다 — 잘 디자인된 마케팅 클레임이 더 효과적이다. (2) AI로 디자인된 성공적 활성 성분은 곧장 특허 자산이 되며, 발표 인센티브가 사라진다. [2]는 이 점을 직설적으로 표현한다 — "bioengineered active의 효능 주장 대부분은 회사 보도자료에 의존하며, 동료 심사 임상에 의존하지 않는다".
화장품 산업의 R&D 기획에 시사: 첫 번째 발표 readout을 만드는 회사는 — 그 active가 마케팅적으로 즉시 성공하지 않더라도 — 카테고리 정의(category-defining) 자산을 갖게 된다. 한국 산업(COSMAX·아모레퍼시픽·LG생활건강) 중 한 곳, 혹은 EU 중견(Lactobio 인수 이전의 patron 형태)이 첫 발표 후보로 보인다. Chapter 9는 그 임상 readout 템플릿을 자세히 다루고, Chapter 12는 이를 산업 전체 청사진의 결정 변수로 통합한다.
4.8 Open Questions
- Endpoint proxy의 타당성 — 항노화에서 procollagen ELISA, MMP-1 발현은 in vivo dermal density·wrinkle depth와 어느 정도 인과적으로 연결되는가? 화장품 ML이 학습하는 proxy의 clinical correlation을 정량화한 외부 연구는 매우 드물다.
- 데이터 규모의 천장 — 50K~100K 샘플 규모의 사내 코호트가 단일 phenotype에서 평탄해지는 시점은 어디인가? Unilever 30K·COSMAX FACE-LINK 950으로는 학습 곡선의 정점이 어디인지 외부에서 추정 불가능하다(Gap 2). 만약 학습 곡선이 100K 전에 평탄해진다면 산업의 데이터 사재기 경쟁은 합리적이지 않다.
- 피부 타입·인종 일반화 — [10]가 명시하듯 cosmetogenomics 연구는 "geographic diversity 제한, darker phototype 과소대표"가 구조적 문제다. 한국 cohort(FACE-LINK)·Chinese cohort(iHSMGC)·Western cohort(HMP)에서 학습된 모델이 다른 인종 group에 일반화될 때 어떻게 성능 저하되는가? 화장품의 글로벌 출시에 직접 영향.
- BGC class 편향 — 현재 ML triage가 잘 작동하는 RiPP·NRPS·PKS는 학습 데이터가 풍부한 클래스다. Cutibacterium·Malassezia 같은 화장품 핵심 균종에서 더 흔한 RiPP·terpene 변종은 모델이 잘 잡지 못할 가능성이 크다 — 이는 곧 신규 발견 영역이기도 하다.
- 검증 자원의 분배 — ML이 100개 후보를 5개로 줄이는 데 성공해도, 그 5개를 임상까지 가져갈 인력·자본은 별개 문제다. 화장품 R&D 조직의 wet-lab 검증 처리량이 ML triage 출력을 모두 받아내지 못한다면 — 가장 가능성 높은 산업 시나리오다 — 다음 병목은 어디로 이동하는가?
참고문헌
- Abramson, J., Adler, J., Dunger, J. et al. (2024). Accurate structure prediction of biomolecular interactions with AlphaFold 3. Nature 630, 493–500.
- Atallah, C., El Abiad, A., El Abiad, M. et al. (2025). Bioengineered Skin Microbiome: The Next Frontier in Personalized Cosmetics. Cosmetics 12(5):205.
- Carrieri, A. P., Haiminen, N., Maudsley-Barton, S. et al. (2021). Explainable AI reveals changes in skin microbiome composition linked to phenotypic differences. Scientific Reports 11:4565.
- Cradle Bio (2024). Cradle's $73M Series B for AI protein design. TechCrunch / SynBioBeta, Nov 2024. [Cradle, 2024]
- Deep learning microbiome review — Wang, T., Yang, L. et al. (2024). Deep learning in microbiome analysis: a comprehensive review of neural network models. Frontiers in Microbiology 15:1516667.
- Di Guardo, A., Trovato, F., Cantisani, C. et al. (2025). Artificial Intelligence in Cosmetic Formulation: Predictive Modeling for Safety, Tolerability, and Regulatory Perspectives. Cosmetics 12(4):157.
- FAST-NPS authors (2025). FAST-NPS — high-throughput automated genome mining for bioactive natural products00040-X). Cell Systems, March 2025. [FAST-NPS, 2025]
- Gueniche, A., Perin, O., Bouslimani, A. et al. (2022). Advances in Microbiome-Derived Solutions and Methodologies Are Founding a New Era in Skin Health and Care. Pathogens 11(2):121.
- Hashimoto, K., Yamamoto, T., Yagi, M. et al. (2022). NRF2 activation by Galactomyces ferment filtrate complements the AHR-axis mechanism in skin barrier homeostasis. Journal of Cosmetic Dermatology, 2022. [Hashimoto et al., 2022]
- Haykal, D., Flament, F., Amar, D. et al. (2025). Cosmetogenomics unveiled: a systematic review of AI, genomics, and the future of personalized skincare. Frontiers in Artificial Intelligence 8:1660356.
- Hayes, T., Rao, R., Akin, H. et al. (2025). Simulating 500 million years of evolution with a language model (ESM3). Science, 2025.
- Insilico Medicine clinical authors, Ren, F., Zhavoronkov, A. et al. (2025). A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine, May 2025. [Insilico, 2025]
- Kim, J., Lee, Y. I., Mun, S. et al. (2023). Efficacy and Safety of Epidermidibacterium Keratini EPI-7 Derived Postbiotics in Skin Aging: A Prospective Clinical Study. International Journal of Molecular Sciences 24(5):4634.
- Wang, X.-W., Wang, T., Liu, Y.-Y. (2024). Artificial Intelligence for Microbiology and Microbiome Research. arXiv preprint 2411.01098. [Wang et al., 2024]
- Krismer, B., Peschel, A. et al. (2024). Commensal production of broad-spectrum antimicrobial peptide polyene eliminates nasal S. aureus (epifadin). Nature Microbiology, 2024.
- Li, Z., Xia, J., Jiang, L. et al. (2021). Characterization of the human skin resistome and identification of two microbiota cutotypes (iHSMGC catalog). Microbiome 9:47.
- L'Oréal R&I Press (2023). L'Oréal acquires Lactobio to strengthen microbiome research. L'Oréal press, Dec 2023; closed Q1 2024. [L'Oréal, 2023]
- Mun, S., Jo, H., Heo, Y. M. et al. (2025). Skin microbiome-biophysical association: a first integrative approach to classifying Korean skin types and aging groups (FACE-LINK). Frontiers in Cellular and Infection Microbiology 15:1561590.
- Novo Nordisk; Cradle (2024). Novo Nordisk × Cradle AI protein design partnership disclosure. Cradle Series B press, Nov 2024. [Novo Nordisk, 2024]
- Papoutsoglou, G., Tarazona, S., Lopes, M. B. et al. (2023). Machine learning approaches in microbiome research: challenges and best practices. Frontiers in Microbiology 14:1261889.
- Pun, F. W., Ozerov, I. V., Zhavoronkov, A. et al. (2024). PandaOmics: An AI-Driven Platform for Therapeutic Target and Biomarker Discovery. Journal of Chemical Information and Modeling, Feb 2024.
- Ren, F., Ding, X., Zheng, M. et al. (2024). A small-molecule TNIK inhibitor (ISM001-055 / rentosertib) discovered via end-to-end generative AI from target identification to Phase 1. Nature Biotechnology, Mar 2024.
- Ruffolo, J. A., Nayfach, S., Gallagher, J. et al. (2024). Design of highly functional genome editors by modeling the universe of CRISPR-Cas proteins (Profluent ProGen2 / OpenCRISPR-1). bioRxiv 2024.04.22.590591.
- Skin Bug authors — Lee, S. et al. (2021). SkinBug — AI prediction of skin microbiome-mediated metabolism of biotics and xenobiotics. iScience 24(1):102026. [SkinBug, 2021]
- Stokes, J. M., Yang, K., Swanson, K. et al. (2020). A Deep Learning Approach to Antibiotic Discovery30102-1). Cell 180(4):688–702.
- Takei, K., Mitoma, C., Hashimoto-Hachiya, A. et al. (2015). Galactomyces ferment filtrate as AHR agonist restoring filaggrin and skin barrier function. Journal of Dermatological Science, 2015. [Takei et al., 2015]
- Unilever Beauty & Wellbeing R&D (2025). How Unilever's pioneering skin microbiome research is shaping product innovation. Unilever news; SXSW 2025 + R&D page coverage. [Unilever, 2025]
- Wang, Y., Liu, R., Chen, S. et al. (2025). Skin microbiome and aging: a review of clinical and molecular evidence. Microbiological Research, 2025. [Wang et al., 2025]
- Zhavoronkov, A., Ivanenkov, Y. A., Aliper, A. et al. (2019). Deep learning enables rapid identification of potent DDR1 kinase inhibitors. Nature Biotechnology 37, 1038–1040.